Đề số 5 - Đề kiểm tra học kì 2 - Hóa học 11
Đáp án và lời giải chi tiết Đề số 5 - Đề kiểm tra học kì 2 (Đề thi học kì 2) - Hóa học 11
Đề bài
I. PHẦN TRẮC NGHIỆM
Câu 1. Đốt cháy một ankan (X), thu được tỉ lệ khối lượng CO2 và nước bằng 11 : 6. Công thức phân tử của (X) là:
A. CH4. B. C2H6.
C. C3H8. D. C4H10.
Câu 2. Đốt cháy hết a lít khí metan rồi cho sản phẩm cháy hấp thụ hết vào 200ml dung dịch Ba(OH)2 0,1M thu được 1,97 gam kết tủa. Hỏi a có giá trị bao nhiêu?
A. 0,560 lít. B. 0,224 lít.
C. 0,672 lít. D. Cả B và C đều đúng.
Câu 3. Nếu cho 1,12 lít propen (đktc) phản ứng với dung dịch nước brom thì lượng brom thì lượng brom tham gia phản ứng tối đa là:
A. 6 gam. B. 16 gam.
C. 9 gam. D. 8 gam.
Câu 4. Khi cho hỗn hợp khí metan và etilen (ở đktc) đi qua dung dịch brom thì lượng brom tham gia phản ứng là 8 gam. Thể tích khí bị brom hấp thụ là:
A. 6,72 lít. B. 5,40 lít.
C. 1,12 lít. D. 10,08 lít.
Câu 5. Cho 13,44 C2H2 (đktc) qua ống đựng than hoạt tính và nung ở \(600^\circ C\) thu được 12,48 gam benzen. Hiệu suất của phản ứng điều chế benzen là:
A. 70%. B. 80%.
C. 82%. D. 95%.
Câu 6. Một hiđrocacbon (X) có công thức nguyên (CH)n. Biết 1 mol (X) phản ứng vừa đủ với 4 mol H2 hoặc với 1 mol Br2 trong dung dịch. Tên gọi của (X) là:
A. benzen. B. Stiren.
C. toluen. D. axetilen.
Câu 7. Một hỗn hợp (Z) chứa một ancol đơn chức, no X và một ancol hai chức no Y. Biết X, Y đều có cùng số nguyên tử cacbon và số mol bằng nhau. Nếu đem đốt cháy hết 0,02 mol (Z) thu được 1,76 gam CO2. Công thức phân tử của hai ancol X và Y lần lượt là:
A. C3H6(OH)2 và C3H5(OH)3.
B. CH3OH và C2H4(OH)2.
C. C2H5OH và C2H4(OH)2.
D. C3H7OH và C3H6(OH)2.
Câu 8. Lấy 11,75 gam phenol cho phản ứng hết với nước brom dư, hiệu suất phản ứng 64%. Khối lượng kết tủa trắng thu được là:
A. 26,48 gam.
B. 64,65 gam.
C. 41,375 gam.
D. Cả A, B và C đều không đúng.
Câu 9. Cho hợp chất (X) có công thức phân tử C8H10O, biết (X) là dẫn xuất của benzen, không tác dụng với NaOH nhưng có khả năng tách nước tạo anken. Hỏi có bao nhiêu đông phân của (X) thỏa mãn điều kiện trên?
A. 2.
B. 3.
C. 4.
D. 5.
Câu 10. Một axit (Y) mạch hở, không phân nhánh có công thức phân tử là (C3H5O2)n. Giá trị của n là:
A. n = 4. B. n = 3.
C. n = 2. D. n = 1.
Câu 11. Số đồng phân anđehit ứng với công thức phân tử C5H10O là:
A.4. B.3.
C.2. D.1.
Câu 12. Nhiệt độ sôi của hợp chất nào sau đây là cao nhất?
A. CH3OH. B. C2H5OH.
C. HCOOH. D. CH3COOH.
II. PHẦN TỰ LUẬN
Câu 13. Có một hỗn hợp X gồm hai hiđrocacbon A và B ở thể khí. Phân tử khối của B lớn hơn phân tử khối của A là 24 u. Tỉ khối hơi so với hiđro của B bằng \(\dfrac{9}{5}\) tỉ khối hơi so với hiđro của A. Hãy xác định công thức phân tử của A và B.
Câu 14. Để làm kết tủa hoàn toàn 7,84 lít hỗn hợp X gồm axetilen và propin (đktc) thì cần vừa đủ 400ml dung dịch AgNO3 1,5M. Hãy xác định khối lượng kết tủa thu được trong hai phản ứng trên.
Câu 15. Cho 3,7 gam ancol no đơn chức X tác dụng hết với kali thu được 700ml khí H2 ở \(27,3^\circ C\) và 668,8mmHg. Xác định công thức phân tử của ancol X đem dùng.
Câu 16. Đốt cháy a mol một axit cacboxylic Z thu được x mol CO2 và y mol H2O. Biết x – y = a. Hãy đề xuất công thức tổng quát của axit Z.
Lời giải chi tiết
I. PHẦN TRẮC NGHIỆM
|
Câu |
1 |
2 |
3 |
4 |
|
Đáp án |
C |
D |
D |
C |
|
Câu |
5 |
6 |
7 |
8 |
|
Đáp án |
B |
B |
C |
A |
|
Câu |
9 |
10 |
11 |
12 |
|
Đáp án |
D |
C |
A |
D |
II. PHẦN TỰ LUẬN
Câu 13.
Gọi phân tử khối của chất A là MA và chất B là MB.
Theo đề ra, ta có: \({M_B} = {M_A} + 25;\dfrac{{{M_B}}}{2} = \dfrac{9}{5}\dfrac{{{M_A}}}{2}\)
\(\begin{array}{l} \Rightarrow \dfrac{{{M_A} + 24}}{2} = \dfrac{9}{5}.\dfrac{{{M_A}}}{2}\\ \Leftrightarrow 5{M_A} + 120 = 9{M_A}\\ \Rightarrow {M_A} = 30(u);{M_B} = 54(u)\end{array}\)
Gọi công thức của A: CxHy (x, y là nguyên dương, \(y \le 2x + 2\))
\( \Rightarrow 12x + y = 30 \Rightarrow y = 30 - 12x \)
\(\Rightarrow x < 2,5 \Rightarrow 1 \le x < 2,5\)
Bảng biện luận:
|
x |
1 |
2 |
3 |
|
y |
18 |
6 |
-6 |
Vậy công thức phân tử của A là: C2H6
Vì MB lớn hơn MA 24 u tức 2 nguyên tử cacbon
Suy ra công thức phân tử của B: C4H6.
Hoặc có thể dựa vào MB để biện luận.
Câu 14.
Ta có: \({n_X} = \dfrac{{7,84}}{{22,4}} = 0,35\left( {mol} \right);\)
\({n_{AgN{O_3}}} = 0,4 \times 1,5 = 0,6\left( {mol} \right)\)
Gọi a là số mol của \(CH \equiv CH\) và b là số mol của \(C{H_3} - C \equiv CH\)
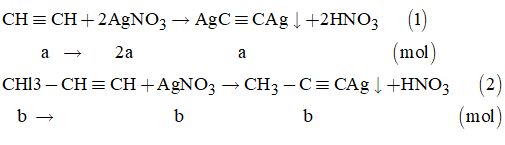
Theo đề bài, ta có hệ phương trình:
\(\left\{ \begin{array}{l}a + b = 0,35\\2a + b = 0,6\end{array} \right. \Rightarrow \left\{ \begin{array}{l}a = 0,25\\b = 0,1\end{array} \right.\)
Từ (1) \( \Rightarrow {n_{{C_3}{H_3}Ag}} = b = 0,1\left( {mol} \right)\)
\( \Rightarrow {m_{{C_3}{H_3}Ag}} = 0,1 \times 147 = 14,7\left( {gam} \right)\)
Vậy \(\sum {{m_{kt}}} = 60 + 14,7 = 74,7\left( {gam} \right)\).
Câu 15.
Ta có:
\({n_{{H_2}}} = \dfrac{{pV}}{{RT}} \)\(\,= \dfrac{{\dfrac{{668,8}}{{760}}}}{{0,082\left( {273 + 27,3} \right)}} \times 0,7\)\(\, = 0,025\left( {mol} \right)\)
Phản ứng:
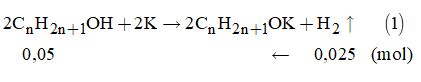
Từ (1) \( \Rightarrow {n_{{C_n}{H_{2n + 1}}OH}} = 0,05\left( {mol} \right)\)
\(\Rightarrow {M_{{C_n}{H_{2n}}OH}} = \dfrac{{3,7}}{{0,05}}\left( u \right).\)
Vậy công thức phân tử của X: C4H9OH.
Câu 16. Phản ứng:
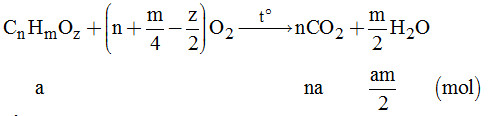
Theo đề bài, ta có: \(x - y = a \Leftrightarrow an - \dfrac{{am}}{2} = a\)
\(\Leftrightarrow m = 2n - 2\)
Vậy công thức phân tử chung của axit là: CnH2n-2Oz.
Search google: "từ khóa + timdapan.com" Ví dụ: "Đề số 5 - Đề kiểm tra học kì 2 - Hóa học 11 timdapan.com"







