Đề thi hóa 10 học kì 2 có đáp án - Đề số 4
Đề thi Hóa học kì 2 lớp 10 năm 2020 - Đề số 4 được đội ngũ giáo viên của TimDapAnbiên soạn nằm trong bộ đề thi trắc nghiệm Hóa 10 kì 2 có đáp án kèm theo, nội dung câu hỏi dưới dạng câu hỏi trắc nghiệm. Bám sát nội dung chương trình cấu trúc đề thi Hóa học 10, giúp các em luyện tập, củng cố câu hỏi lý thuyết, các dạng bài tập. Hi vọng tài liệu này giúp các em có thể đạt được kết quả tốt trong kì thi.
- Đề thi lớp 10 cuối kì 2 năm 2020 môn Hóa học (số 1)
- Đề thi lớp 10 cuối kì 2 năm 2020 môn Hóa học (số 2)
- Đề thi Hóa học kì 2 lớp 10 năm 2020 - Đề số 5
- Ôn tập Hóa học 10 kì 2 năm 2019 - 2020
ĐỀ KIỂM TRA CUỐI KÌ 2 MÔN HÓA HỌC LỚP 10
Bản quyền thuộc về TimDapAnnghiêm cấm mọi hành vi sao chép vì mục đích thương mại
(Cho Fe = 56; Na = 23; Ca = 40; Mg = 24; Mn = 55; Cu = 64; Al = 27, Zn = 65, S = 32, O = 16; Cl = 35,5; Ag = 108; H = 1)
Câu 1. Số oxi hoá của clo trong các chất: NaCl, NaClO, KClO3, Cl2, KClO4 lần lượt là:
A. –1, +1, +3, 0, +7.
B. –1, +1, +5, 0, +7.
C. –1, +3, +5, 0, +7.
D. +1, –1, +5, 0, +3.
Câu 2. Khí nào sau đây có khả năng làm mất màu nước brom?
A. N2.
B. CO2.
C. H2.
D. SO2.
Câu 3. Sục khí clo vào lượng dung dịch NaOH ở nhiệt độ thường, sản phẩm là
A. NaCl, NaClO.
B. NaCl, NaClO2.
C. NaCl, NaClO3.
D. Chỉ có NaCl.
Câu 4. Khi phản ứng thuận nghịch ở trạng thái cân bằng thì nó:
A. Không xảy ra nữa
B. Vẫn tiếp tục xảy ra
C. Chỉ xảy ra theo chiều thuận
D. Chỉ xảy ra theo chiều nghịch
Câu 5. Có 4 dung dịch NaF, NaCl, NaBr, NaI đựng trong các lọ bị mất nhãn. Nếu dùng dung dịch AgNO3 thì có thể nhận biết được
A. 1 dung dịch
B. 2 dung dịch
C. 3 dung dịch
D. 4 dung dịch
Câu 6. Hóa chất nào sau đây không được đựng bằng lọ thủy tinh?
A. HNO3.
B. HF.
C. HCl.
D. NaOH.
Câu 7. Cho sơ đồ:
Cl2 + KOH A + B + H2O
Cl2 + KOH A + C + H2O
Công thức hoá học của A, B, C, lần lượt là:
A. KCl, KClO, KClO4.
B. KClO3, KCl, KClO.
C. KCl, KClO, KClO3.
D. KClO3, KClO4, KCl.
Câu 8. Lưu huỳnh tác dụng với dung dịch kiềm nóng theo phản ứng sau:
S + KOH K2S + K2SO3 + H2O
Tỉ lệ số nguyên tử lưu huỳnh bị oxi hóa và số nguyên tử lưu huỳnh bị khử là:
A. 2 : 1
B. 1 : 2
C. 1 : 3
D. 2 : 3
Câu 9. Dẫn 1,12 lít khí SO2 (đktc) vào 200ml dung dịch NaOH 1M, dung dịch được có chứa
A. NaHSO3
B. NaHSO3 và Na2SO3
C. Na2SO3 và NaOH
D. Na2SO3
Câu 10. Cho 10 gam hỗn hợp Fe, FeO, Fe2O3 tác dụng với dung dịch H2SO4 loãng dư, thấy có 3,36 lít khí thoát ra (đktc). Thành phần % khối lượng của Fe trong hỗn hợp là:
A. 84%
B. 8,4 %
C. 48%
D. 42%
Câu 11. Biết tỉ khối hơi của hỗn hợp Y gồm oxi và ozon đối với khí metan là 2,4. Phần trăm theo thể tích của mỗi khí trong hỗn hợp Y là:
A. 40%, 60%
B. 70%, 30%
C. 50%, 50%
D.45%, 55%
Câu 12. Cho phản ứng sau: Các chất phản ứng → các chất sản phẩm. Yếu tố không ảnh hưởng đến tốc độ phản ứng nói trên là:
A. Nồng độ các chất phản ứng
B. Nồng độ các chất sản phẩm
C. Nhiệt độ
D. Chất xúc tác
Câu 13. Cho hỗn hợp gồm Fe và FeS hòa tan vào dung dịch HCl dư thu được 6,72 lít hỗn hợp khí (đktc). Dẫn toàn bộ hỗn hợp này qua dung dịch Pb(NO3)2 dư thu được 47,8 gam kết tủa đen. % khối lượng Fe và FeS có trong hỗn hợp ban đầu là:
A. 25,2%; 74,8%
B. 24,14%; 78,86%
C. 32%; 68%
D. 60%; 40%
Câu 14. Thể tích khí thu được sau phản ứng khi cho 6,5 gam Zn tác dụng với axit H2SO4 đặc nóng
A. 4,48 lít
B. 2,24 lít
C. 3,36 lít
D. 1,12 lít
Câu 15. 16,5 gam hỗn hơp Mg, Fe, Zn tác dụng vừa đủ với dung dịch H2SO4 loãng thấy thoát ra 4,48 lít khí H2 đktc). Sau phản ứng cô cạn thu được khối lượng muối khan là:
A. 34,3 gam
B. 43,3 gam
C. 35,7 gam
A. 33,8 gam
Câu 16. Có 5 lọ mất nhãn có các muối NaCl, KNO3, Pb(NO3)2, CuSO4, FeCl2. Khi sục khí H2S qua các dung dịch muối trên, có bao nhiêu trường hợp có phản ứng sinh ra kết tủa?
A. 1
B. 2
C. 4
D. 3
Câu 17. Trong gia đình, nồi áp suất được sử dụng để nấu chín kỹ thức ăn. Lí do nào sau đây là thích hợp cho việc sử dụng nồi áp suất?
A. Tăng áp suất và nhiệt độ lên thức ăn.
B. Giảm hao phí năng lượng.
C. Giảm thời gian nấu ăn.
D. Cả A, B và C đúng.
Câu 18. Hòa tan hoàn toàn 11,2 gam kim loại A có hóa trị II vào H2SO4 loãng thu được 4,48 lít H2 (đktc). Kim loại A là:
A. Mg
B. Zn
C. Cu
D. Fe
Câu 19. Khi tăng thêm 10oC, tốc độ phản ứng hóa học tăng lên 4 lần. Vậy khi giảm nhiệt độ từ 70oC xuống 40oC thì tốc độ phản ứng giảm đi
A. 32 lần
B. 64 lần
C. 128 lần
D. 16 lần
Câu 20. Sản phẩm tạo thành của phản ứng giữa Fe3O4 với H2SO4 đặc, nóng, dư là:
A. Fe2(SO4)3, SO2, H2O
B. Fe2(SO4)3, H2O
C. FeSO4, SO2, H2O
D. FeSO4, Fe2(SO4)3
Câu 21. So sánh tốc độ của 2 phản ứng sau (thực hiện ở cùng nhiệt độ, thành phần Zn như nhau):
Zn + dung dịch CuSO4 1M (1)
Zn + dung dịch CuSO4 2M (2)
Kết quả thu được là:
A. 1 nhanh hơn 2.
B. 2 nhanh hơn 1.
C. như nhau.
D. không xác định.
Câu 22. Có 2 dung dịch axit HCl có nồng độ 10% và 3%. Để thu được dung dịch axit HCl mới có nồng độ 5% thì phải trộn chúng theo tỉ lệ khối lượng là:
A. 2:2
B. 2:3
C. 2:5
D. 2:4
Câu 23. Khí HCl khô khi gặp quỳ tím thì làm quỳ tím
A. chuyển sang màu đỏ.
B. chuyển sang màu xanh.
C. không chuyển màu.
D. chuyển sang không màu.
Câu 24. Các chất trong nhóm nào sau đây đều tác dụng với dung dịch HCl?
A. Quỳ tím, SiO2, Fe(OH)3, Zn, Na2CO3.
B. Quỳ tím, CuO, Cu(OH)2, Zn, Na2CO3.
C. Quỳ tím, CaO, NaOH, Ag, CaCO3.
D. Quỳ tím, FeO, NH3, Cu, CaCO3.
Câu 25. Hòa tan toàn 13,76 gam hỗn hợp X gồm hai muối NaCl và NaBr vào nước thu được dung hoàn dịch X. Cho khí clo lội từ từ cho đến dư qua dung dịch X thu được dung dịch Y. Làm bay hơi dung dịch Y cho tới khi thu được 12,87 gam muối khan B. Khối lượng của NaCl trong hỗn hợp X là
A. 11,7 gam
B. 5,85 gam
C. 8,77 gam
D. 9,3 gam
ĐÁP ÁN ĐỀ KIỂM TRA CUỐI KÌ 2 MÔN HÓA HỌC LỚP 10
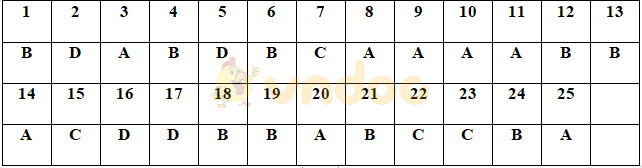 TimDapAnđã giới thiệu Đề thi Hóa học kì 2 lớp 10 năm 2020 - Đề số 4 có đáp án kèm theo, gồm 25 câu hỏi lý thuyết, bài tập tính toán dưới dạng trắc nghiệm, bám sát nội dung ôn tập Hóa 10 học kì 2, các dạng bài tập tính toán tổng hợp. Giúp các em ôn luyện tốt hơn để làm bài thi hóa kì 2 lớp 10 tự tin, đạt kết quả tốt nhất.
TimDapAnđã giới thiệu Đề thi Hóa học kì 2 lớp 10 năm 2020 - Đề số 4 có đáp án kèm theo, gồm 25 câu hỏi lý thuyết, bài tập tính toán dưới dạng trắc nghiệm, bám sát nội dung ôn tập Hóa 10 học kì 2, các dạng bài tập tính toán tổng hợp. Giúp các em ôn luyện tốt hơn để làm bài thi hóa kì 2 lớp 10 tự tin, đạt kết quả tốt nhất.
Trên đây Tìm Đáp Án đã giới thiệu tới các bạn Đề thi Hóa học kì 2 lớp 10 năm 2020 - Đề số 4. Để có kết quả học tập tốt và hiệu quả hơn, TimDapAnxin giới thiệu tới các bạn học sinh tài liệu Giải bài tập Toán 10, Chuyên đề Vật Lí 10, Giải bài tập Sinh học 10, Chuyên đề Hóa học 10. Tài liệu học tập lớp 10 mà TimDapAntổng hợp biên soạn và đăng tải.











