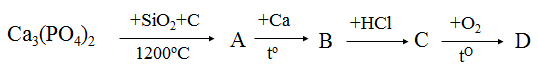Bài 10: Photpho
Video 1: Giới thiệu về Phopho
1. Vị trí và cấu hình electron nguyên tử
- Cấu hình e: 1s2 2s2 2p6 3s2 3p3.
- Ví trí: Z = 15, chu kì 3, nhóm VA
- Hoá trị có thể có của P: 5 và 3
2. Tính chất vật lí
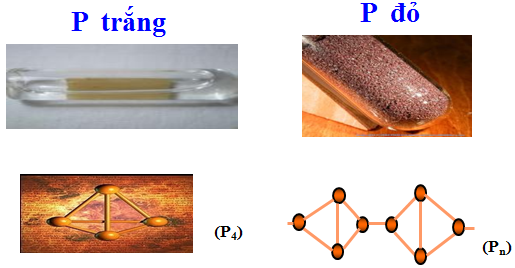
Hình 1: P trắng và P đỏ
- P trắng:
+ Trạng thái - màu sắc: Chất rắn, trong suốt, màu trắng hoặc hơi vàng
+ Tính tan: Không tan trong nước
+ Tính độc - Tính bền: Không độc - Bền ở điều kiện thường
+ Tính phát quang: Phát quang màu lục nhạt trong bóng tối
- P đỏ:
+ Trạng thái - màu sắc: Chất bột, màu đỏ
+ Tính tan: Không tan trong các dung môi thường
+ Tính độc - Tính bền: Rất độc, gây bỏng nặng khi rơi vào da - Không bền, dễ bốc cháy trong không khí
+ Tính phát quang: Không phát quang trong bóng tối
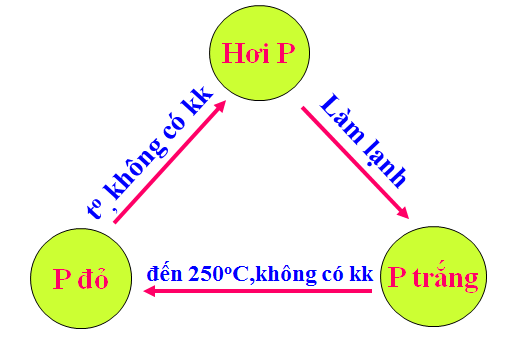
Hình 2: Sơ đồ chuyển hóa giữa Photpho trắng và Photpho đỏ
3. Tính chất hóa học
3.1. Tính oxi hoá
P + 3Na → Na3P
2P + 3Ca → Ca3P2 (canxi photphua)
2P + 3Zn → Zn3P2 (Kẽm photphua)
3.2. Tính khử
- Khi tác dụng với phi kim hoạt động và những chất oxi hoá mạnh.
- Với oxi:
5O2 (dư) + 4P → 2P2O5 (Điphotpho pentaoxit)
3O2 (thiếu) + 4P → 2P2O3 (Điphotpho trioxit)
Video 2: Phản ứng giữa Photpho và Oxi
- Với clo:
5Cl2 (dư) +2P → 2PCl5 (photpho pentaclorua)
3Cl2 (thiếu) + 2P → 2PCl3 (photpho triclorua)
- Với hợp chất: P + 5HNO3 đ,n → H3PO4 + 5NO2 + H2O
4. Ứng dụng
Hình 3: Ứng dụng của photpho
5. Trạng thái tự nhiên
Hình 4: Hai khoáng vật chính của photpho
6. Sản xuất
- Trong công nghiệp, photpho đỏ được sản xuất bằng cách nung hỗn hợp quặng photphorit (hoặc apatit), cát và than cốc ở 12000C trong lò điện.
Ca3(PO4)2 + 3 SiO2 + 5C → 5CO + 2Phơi + 3CaSiO3
- Lào Cai là một trong những tỉnh giàu tài nguyên khoáng sản nhất Việt Nam với 35 loại khoáng sản khác nhau. Trong đó có nhiều loại khoáng sản như apatít, đồng, sắt, graphít, nguyên liệu cho gốm, sứ, thuỷ tinh,… với trữ lượng lớn nhất cả nước.
7. Tổng kết
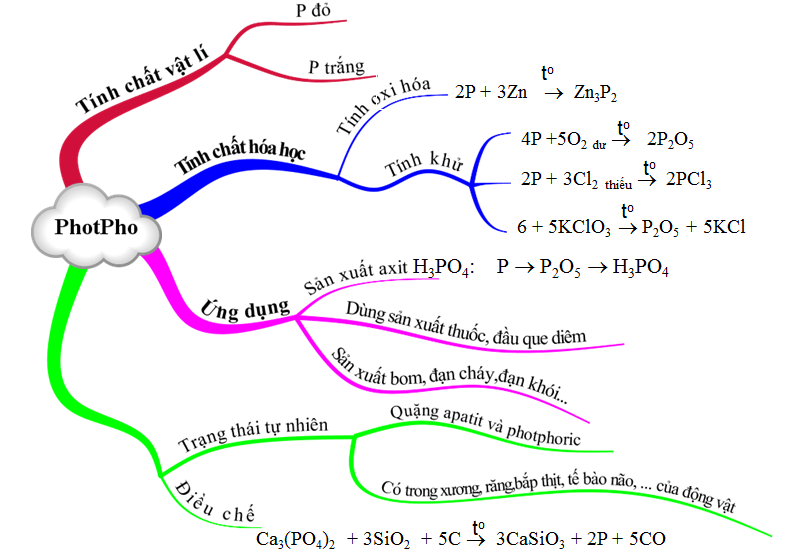
Hình 5: Sơ đồ tư duy bài Photpho
Bài 1:
Chọn một phương án đúng để điền cụm từ vào chỗ trống khi so sánh tính chất vật lí của P trắng và P đỏ sau:
- P trắng:
+ Trạng thái, màu sắc: ...
+ Cấu trúc phân tử: ...
+ Tính tan: ...
+ Tính độc: ...
+ Tính bền: ...
+ Khả năng phát quang: ...
- P đỏ:
+ Trạng thái, màu sắc: ...
+ Cấu trúc phân tử: ...
+ Tính tan: ...
+ Tính độc: ...
+ Tính bền: ...
+ Khả năng phát quang: ...
(1) chất rắn, trong suốt, màu trắng hoặc vàng nhạt
(2) cấu trúc polime (Pn)
(3) không tan trong nước, tan trong dung môi hữu cơ
(4) chất bột, màu đỏ
(5) phát quang màu lục nhạt trong bóng tối
(6) không độc
(7) không tan trong các dung môi thông thường
(8) bền ở nhiệt độ thường.
(9) không phát quang trong bóng tối
(10) không bền.
(11) rất độc, gây bỏng nặng khi rơi vào da.
(12) cấu trúc mạng tinh thể ptử (P4)
Hướng dẫn:
- P trắng:
+ Trạng thái, màu sắc: (1)
+ Cấu trúc phân tử: (12)
+ Tính tan: (3)
+ Tính độc: (11)
+ Tính bền: (10)
+ Khả năng phát quang: (5)
- P đỏ:
+ Trạng thái, màu sắc: (4)
+ Cấu trúc phân tử: (2)
+ Tính tan: (7)
+ Tính độc: (6)
+ Tính bền: (8)
+ Khả năng phát quang: (9)
Bài 2:
Giải thích tại sao ở điều kiện thường photpho hoạt động hơn nitơ mặc dù độ âm điện của photpho (2,19) nhỏ hơn độ âm điện của nitơ (3,04)?
Hướng dẫn:
Liên kết trong phân tử photpho là liên kết đơn, kém bền vững hơn liên kết ba trong phân tử nitơ. Vì vậy ở điều kiện thường photpho hoạt động hơn nitơ.
Bài 3:
Dựa vào khả năng bốc cháy khác nhau của photpho trắng và photpho đỏ, cho biết dạng thù hình nào của photpho hoạt động mạnh hơn?
Hướng dẫn:
P trắng hoạt động hóa học mạnh hơn P đỏ.
Bài 4:
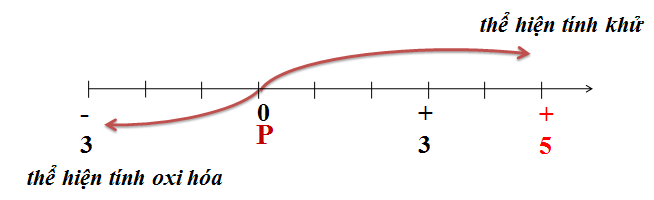
Cho các chất sau: Ca3P2, P, P2O3, PCl5, H3PO4.
Hãy xác định số oxi hóa của P.
Cho biết các số oxi hoá có thể có của photpho trong hợp chất. Từ đó dự đoán tính chất hoá học của photpho?
Hướng dẫn:
Số oxi hóa của P ở các chất Ca3P2, P, P2O3, PCl5, H3PO4 lần lượt là: (-3), (0), (+3), (+5), (+5)
Bài 5:
Hoàn thành sơ đồ phản ứng sau: Với D là hợp chất của Photpho
Hướng dẫn:
Các phương trình phản ứng như sau:
Ca3(PO4)2 + 3SiO2 + 5C → 3CaSiO3 + 2P + 5CO
2P + 3Ca → Ca3P2
Ca3P2 + 6HCl → 3CaCl2 + 2PH3
2PH3 + 4O2 → P2O5 + 3H2O
Vậy A là Phopho, B là Ca3P2, C là PH3, D là P2O5
Bài 6:
Nhận định nào đúng, nhận định nào sai trong các nhận định sau?
1. P ở ô thứ 15, chu kì 3, nhóm VA
2. Bảo quản P trắng bằng cách đậy kín trong lọ có không khí
3. P đỏ hoạt động mạnh hơn P trắng
4. Trong hợp chất, P có số oxi hóa: -3, +3 và +5
5. P chỉ thể hiện tính oxi hóa khi tác dụng với oxi
6. P đỏ phát quang màu lục nhạt trong bóng tối
Hướng dẫn:
1. Đúng
2. Sai
3. Sai
4. Đúng
5. Sai
6. Sai
Video 1: Giới thiệu về Phopho
1. Vị trí và cấu hình electron nguyên tử
- Cấu hình e: 1s2 2s2 2p6 3s2 3p3.
- Ví trí: Z = 15, chu kì 3, nhóm VA
- Hoá trị có thể có của P: 5 và 3
2. Tính chất vật lí
Hình 1: P trắng và P đỏ
- P trắng:
+ Trạng thái - màu sắc: Chất rắn, trong suốt, màu trắng hoặc hơi vàng
+ Tính tan: Không tan trong nước
+ Tính độc - Tính bền: Không độc - Bền ở điều kiện thường
+ Tính phát quang: Phát quang màu lục nhạt trong bóng tối
- P đỏ:
+ Trạng thái - màu sắc: Chất bột, màu đỏ
+ Tính tan: Không tan trong các dung môi thường
+ Tính độc - Tính bền: Rất độc, gây bỏng nặng khi rơi vào da - Không bền, dễ bốc cháy trong không khí
+ Tính phát quang: Không phát quang trong bóng tối
Hình 2: Sơ đồ chuyển hóa giữa Photpho trắng và Photpho đỏ
3. Tính chất hóa học
3.1. Tính oxi hoá
P + 3Na → Na3P
2P + 3Ca → Ca3P2 (canxi photphua)
2P + 3Zn → Zn3P2 (Kẽm photphua)
3.2. Tính khử
- Khi tác dụng với phi kim hoạt động và những chất oxi hoá mạnh.
- Với oxi:
5O2 (dư) + 4P → 2P2O5 (Điphotpho pentaoxit)
3O2 (thiếu) + 4P → 2P2O3 (Điphotpho trioxit)
Video 2: Phản ứng giữa Photpho và Oxi
- Với clo:
5Cl2 (dư) +2P → 2PCl5 (photpho pentaclorua)
3Cl2 (thiếu) + 2P → 2PCl3 (photpho triclorua)
- Với hợp chất: P + 5HNO3 đ,n → H3PO4 + 5NO2 + H2O
4. Ứng dụng
Hình 3: Ứng dụng của photpho
5. Trạng thái tự nhiên
Hình 4: Hai khoáng vật chính của photpho
6. Sản xuất
- Trong công nghiệp, photpho đỏ được sản xuất bằng cách nung hỗn hợp quặng photphorit (hoặc apatit), cát và than cốc ở 12000C trong lò điện.
Ca3(PO4)2 + 3 SiO2 + 5C → 5CO + 2Phơi + 3CaSiO3
- Lào Cai là một trong những tỉnh giàu tài nguyên khoáng sản nhất Việt Nam với 35 loại khoáng sản khác nhau. Trong đó có nhiều loại khoáng sản như apatít, đồng, sắt, graphít, nguyên liệu cho gốm, sứ, thuỷ tinh,… với trữ lượng lớn nhất cả nước.
7. Tổng kết
Hình 5: Sơ đồ tư duy bài Photpho
Bài 1:
Chọn một phương án đúng để điền cụm từ vào chỗ trống khi so sánh tính chất vật lí của P trắng và P đỏ sau:
- P trắng:
+ Trạng thái, màu sắc: ...
+ Cấu trúc phân tử: ...
+ Tính tan: ...
+ Tính độc: ...
+ Tính bền: ...
+ Khả năng phát quang: ...
- P đỏ:
+ Trạng thái, màu sắc: ...
+ Cấu trúc phân tử: ...
+ Tính tan: ...
+ Tính độc: ...
+ Tính bền: ...
+ Khả năng phát quang: ...
(1) chất rắn, trong suốt, màu trắng hoặc vàng nhạt
(2) cấu trúc polime (Pn)
(3) không tan trong nước, tan trong dung môi hữu cơ
(4) chất bột, màu đỏ
(5) phát quang màu lục nhạt trong bóng tối
(6) không độc
(7) không tan trong các dung môi thông thường
(8) bền ở nhiệt độ thường.
(9) không phát quang trong bóng tối
(10) không bền.
(11) rất độc, gây bỏng nặng khi rơi vào da.
(12) cấu trúc mạng tinh thể ptử (P4)
Hướng dẫn:
- P trắng:
+ Trạng thái, màu sắc: (1)
+ Cấu trúc phân tử: (12)
+ Tính tan: (3)
+ Tính độc: (11)
+ Tính bền: (10)
+ Khả năng phát quang: (5)
- P đỏ:
+ Trạng thái, màu sắc: (4)
+ Cấu trúc phân tử: (2)
+ Tính tan: (7)
+ Tính độc: (6)
+ Tính bền: (8)
+ Khả năng phát quang: (9)
Bài 2:
Giải thích tại sao ở điều kiện thường photpho hoạt động hơn nitơ mặc dù độ âm điện của photpho (2,19) nhỏ hơn độ âm điện của nitơ (3,04)?
Hướng dẫn:
Liên kết trong phân tử photpho là liên kết đơn, kém bền vững hơn liên kết ba trong phân tử nitơ. Vì vậy ở điều kiện thường photpho hoạt động hơn nitơ.
Bài 3:
Dựa vào khả năng bốc cháy khác nhau của photpho trắng và photpho đỏ, cho biết dạng thù hình nào của photpho hoạt động mạnh hơn?
Hướng dẫn:
P trắng hoạt động hóa học mạnh hơn P đỏ.
Bài 4:
Cho các chất sau: Ca3P2, P, P2O3, PCl5, H3PO4.
Hãy xác định số oxi hóa của P.
Cho biết các số oxi hoá có thể có của photpho trong hợp chất. Từ đó dự đoán tính chất hoá học của photpho?
Hướng dẫn:
Số oxi hóa của P ở các chất Ca3P2, P, P2O3, PCl5, H3PO4 lần lượt là: (-3), (0), (+3), (+5), (+5)
Bài 5:
Hoàn thành sơ đồ phản ứng sau: Với D là hợp chất của Photpho
Hướng dẫn:
Các phương trình phản ứng như sau:
Ca3(PO4)2 + 3SiO2 + 5C → 3CaSiO3 + 2P + 5CO
2P + 3Ca → Ca3P2
Ca3P2 + 6HCl → 3CaCl2 + 2PH3
2PH3 + 4O2 → P2O5 + 3H2O
Vậy A là Phopho, B là Ca3P2, C là PH3, D là P2O5
Bài 6:
Nhận định nào đúng, nhận định nào sai trong các nhận định sau?
1. P ở ô thứ 15, chu kì 3, nhóm VA
2. Bảo quản P trắng bằng cách đậy kín trong lọ có không khí
3. P đỏ hoạt động mạnh hơn P trắng
4. Trong hợp chất, P có số oxi hóa: -3, +3 và +5
5. P chỉ thể hiện tính oxi hóa khi tác dụng với oxi
6. P đỏ phát quang màu lục nhạt trong bóng tối
Hướng dẫn:
1. Đúng
2. Sai
3. Sai
4. Đúng
5. Sai
6. Sai


.PNG)