Đề thi học kì 2 môn Hóa học lớp 11
Đề thi học kì 2 môn Hóa học lớp 11 trường THPT Trần Hưng Đạo, TP Hồ Chí Minh năm học 2015 - 2016 được Tìm Đáp Án sưu tầm và đăng tải, giúp các bạn học sinh luyện tập và củng cố kiến thức môn Hóa hữu ích, từ đó, chuẩn bị sẵn sàng cho kì thi cuối năm môn Hóa tốt nhất. Mời các bạn tham khảo.
Đề thi học kì 2 môn Hóa học lớp 11 trường THPT Đa Phúc, Hà Nội năm học 2015 - 2016
Đề thi học kì 2 môn Hóa học lớp 11 Nâng cao trường THPT Chuyên Huỳnh Mẫn Đạt, Kiên Giang năm 2015
|
SỞ GD & ĐT TP. HỒ CHÍ MINH TRƯỜNG THPT TRẦN HƯNG ĐẠO |
ĐỀ THI HỌC KỲ II MÔN HÓA HỌC - KHỐI 11 Ngày thi: 04/05/2016 Thời gian làm bài: 45 phút |
Câu 1: (2 điểm) Thưc hiện chuỗi phương trình phản ứng sau (ghi rõ điều kiện nếu có):
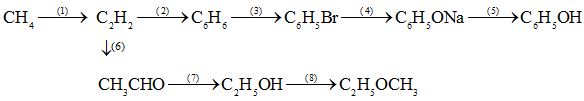
Câu 2: (2 điểm) Nhận biết các chất lỏng đựng trong các lọ mất nhãn sau: Ancol etylic, phenol, axit fomic, axit axetic, glixerol. Viết các phương trình phản ứng xảy ra.
Câu 3: (2 điểm)
a) Viết CTCT thu gọn các đồng phân anđehit có CTPT C5H10O.
b) Từ canxicacbua và các hóa chất vô cơ cần thiết khác hãy viết các phương trình phản ứng điều chế ancol etylic và axit axetic.
Câu 4: (2 điểm) Đốt cháy hoàn toàn hỗn hợp X gồm 2 ancol đơn chức liên tiếp thuộc cùng dãy đồng đẳng thu được 13,2g CO2 và 8,28g H2O. (C = 12, H = 1, O = 16, Na = 23)
a) Tìm công thức phân tử của 2 ancol. Tìm % theo khối lượng 2 ancol trong hỗn hợp ban đầu.
b) Cũng lượng hỗn hợp 2 ancol trên khi cho qua bình đựng Na (dư) thấy khối lượng bình tăng lên m gam. Tính m.
Câu 5: (2 điểm) Cho 22,6 g hỗn hợp X gồm ancol etylic và andehyt axetic tác dụng Natri thu được 3,36 lít khí H2 (đkc). Chất còn lại cho tác dụng dung dịch AgNO3 trong NH3, đun nóng thu được m1 g kết tủa Ag và m2 g muối amoni của axit hữu cơ.
a) Tìm m1 và m2
b) Nếu lấy ½ hỗn hợp X trên đem đốt cháy hoàn toàn rồi dẫn sản phẩm cháy qua bình đựng dung dịch Ca(OH)2 dư thấy khối lượng bình tăng m g. Tìm m
(Biết C = 12, H = 1, O = 16, Na = 23, Ca = 40, N = 14)
Đáp án đề thi học kì 2 môn Hóa học lớp 11
Câu 1: 0,25đ/1pt (trừ ½ số điểm nếu thiếu điều kiện/cân bằng hoặc viết dưới dạng công thức phân tử)
Câu 2: 0,5đ/1chất nếu hiện tượng đúng, phương trình đúng. Chất cuối không có điểm.
Hiện tượng đúng, phương trình sai → chấm hiện tượng
Hiện tượng sai, phương trình đúng → bỏ.
Câu 3: (2 điểm):
a) Mỗi đồng phân + tên gọi: 0,25đ * 4
b) Mỗi phương trình: 0,25đ * 4
Câu 4: (2 điểm)
a) Tính được nCO2 = 0,3 mol, nH2O = 0,46 mol
Tính được nancol = 0,16 mol (0,25đ)
Tính được ![]() (0,25đ)
(0,25đ)
Suy ra công thức CH3OH và C2H5OH (0,25đ)
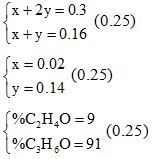
b) Khối lượng bình tăng = khối lượng ancol – khối lượng hiđro
Tính được mancol = 7,08g, mhiđro = 0,16g
Đáp án = 6,92 g 0,5đ
Câu 5 (2 điểm)
a/ nH2 = 0,15mol → nC2H5OH = 0,3mol (0,25đ)
mC2H5OH = 13,8g → mCH3CHO = 8,8g (0,25đ)
nCH3CHO = 0,2mol → nAg = 0,4mol (0,25đ)
m1 = 43,2g (0,25đ)
m2 = 15,4g (0,25đ)
b/ nC2H5OH = 0,15 mol, nCH3CHO = 0,1 mol (0,25đ)
nCO2 = 0,5 mol, nH2O = 0,65 mol (0,25đ)
mbình tăng = mCO2 + mH2O = 33,7g (0,25đ)











