Đề thi học sinh giỏi lớp 9 môn Hóa học
Tuyển tập 30 đề thi học sinh giỏi Hóa học lớp 9 dưới đây sẽ giúp các em học sinh lớp 9 ôn thi học sinh giỏi, thi hết học kì 1 môn Hóa học hiệu quả hơn. Mời các em tải đề thi học sinh giỏi Hóa học lớp 9 dưới đây về để luyện tập.
Mời các bạn tham khảo một số đề thi học sinh giỏi mới nhất:
- Đề thi học sinh giỏi môn Hóa học 9 năm 2020
- Đề thi học sinh giỏi Hóa 9 năm 2020 - Đề số 2
Đề số 1
Câu 1. (6,5 điểm)
1. Khi cho bột nhôm tác dụng với dung dịch NaOH đun nóng thu được dung dịch X1 và khí X2. Thêm vào X1 một ít tinh thể NH4Cl rồi tiếp tục đun nóng thấy tạo thành kết tủa X3 và có khí X4 thoát ra. Xác định X1, X2, X3, X4. Viết phương trình hoá học biểu diễn các phản ứng xảy ra.
2. Xác định các chất A, B, C, D, E, F, H và hoàn thành sơ đồ biến hóa sau:
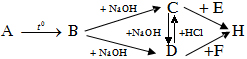
Biết rằng H là thành phần chính của đá phấn; B là khí dùng nạp cho các bình chữa cháy (dập tắt lửa).
3. a. Bằng phương pháp hóa học hãy tách SO2 ra khỏi hỗn hợp gồm các khí SO2, SO3, O2.
b. Bằng phương pháp hóa học hãy tách riêng từng kim loại ra khỏi hỗn hợp gồm Mg, Al, Fe, Cu.
4. Có 5 chất rắn: BaCl2, Na2SO4, CaCO3, Na2CO3, CaSO4.2H2O đựng trong 5 lọ riêng biệt. Hãy tự chọn 2 chất dùng làm thuốc thử để nhận biết các chất rắn đựng trong mỗi lọ.
Câu 2: (5,5 điểm)
1. Viết công thức cấu tạo các đồng phân ứng với công thức phân tử: C2H4O2, C3H8O, C5H10.
2. Chất A có công thức phân tử C4H6. Xác định công thức cấu tạo của A, B, C, D và hoàn thành phương trình hóa học biểu diễn các phản ứng theo sơ đồ:
![]()
3. Hỗn hợp khí gồm CO, CO2, C2H4 và C2H2. Trình bày phương pháp dùng để tách từng khí ra khỏi hỗn hợp
Câu3: (4,0 điểm)
Có hai dung dịch; H2SO4 (dung dịch A), và NaOH (dung dịch B). Trộn 0,2 lít dung dịch A với 0,3 lít dung dịch B được 0,5 lít dung dịch C.
Lấy 20 ml dung dịch C, thêm một ít quì tím vào, thấy có màu xanh. Sau đó thêm từ từ dung dịch HCl 0,05M tới khi quì tím đổi thành màu tím thấy hết 40 ml dung dịch axit.
Trộn 0,3 lít A với 0,2 lít B được 0,5 lít dung dịch D. Lấy 20 ml dung dịch D, thêm một ít quì tím vào thấy có màu đỏ. Sau đó thêm từ từ dung dịch NaOH 0,1M tới khi quì tím đổi thành màu tím thấy hết 80 ml dung dịch NaOH.
a. Tính nồng độ mol/l của 2 dung dịch A và B.
b. Trộn VB lít dung dịch NaOH vào VA lít dung dịch H2SO4 ở trên ta thu được dung dịch E. Lấy V ml dung dịch E cho tác dụng với 100 ml dung dịch BaCl2 0,15 M được kết tủa F. Mặt khác lấy V ml dung dịch E cho tác dụng với 100 ml dung dịch AlCl3 1M được kết tủa G. Nung F hoặc G ở nhiệt độ cao đến khối lượng không đổi thì đều thu được 3,262gam chất rắn. Tính tỉ lệ VB:VA
Câu 4: (4,0 điểm)
Đốt cháy hoàn toàn 3,24 gam hỗn hợp X gồm hai chất hữu cơ A và B khác dãy đồng đẳng và cùng loại hợp chất, trong đó A hơn B một nguyên tử cacbon, người ta chỉ thu được nước và 9,24 gam CO2. Biết tỉ khối hơi của X đối với H2 là 13,5.
a. Tìm công thức cấu tạo của A, B và tính thành phần trăm theo khối lượng của mỗi chất trong hỗn hợp X.
b. Từ B viết sơ đồ phản ứng điều chế CH3COOCH3 và ![]()
Đề số 2
Câu 1. Hoàn thành sơ đồ bằng phương trình phản ứng:
FeS2 +O2 A↑ + B J
B + D
A + H2S C↓+ D L + B
E + D
C + E F F + HCl
G + H2S↑
G + NaOH H↓+ I H + O2 + D
J↓
Câu 2.
a) Cho các chất: Na, MgCl2, FeCl2, FeCl3, AlCl3 chỉ dùng thêm nước hãy nhận biết chúng
b) Có 3 lọ đựng ba hỗn hợp dạng bột: ( Al + Al2O3), (Fe + Fe2O3) và (FeO + Fe2O3). Dùng phương pháp hóa học để nhận biết chúng. Viết phương trình hoá học xảy ra.
Câu 3. Cho hỗn A gồm 3 oxit: Al2O3, CuO và K2O. Tiến hành 3 thí nghiệm:
- Thí nghiệm 1: nếu cho hỗn hợp A vào nước dư, khuấy kĩ thấy còn 15g chất rắn không tan.
- Thí nghiệm 2: Nếu cho thêm vào hỗn hợp A một lượng Al2O3 bằng 50% lượng Al2O3 trong A ban đầu rồi lại hòa tan vào nước dư. Sau thí nghiệm còn lại 21g chất rắn không tan.
- Thí nghiệm 3: Nếu cho vào hỗn hợp A một lượng Al2O3 bằng 75% lượng Al2O3 trong A, rồi lại hòa tan vào nước dư, thấy còn lại 25g chất rắn không tan.
Tính khối lượng oxit trong hỗn hợp A.
Câu 4. Đốt cháy hết V lít (đktc) hỗn hợp CH4 và C2H4, cho toàn bộ sản phẩm thu được hấp thụ hết vào 100ml dung dịch NaOH 1M, thu được dung dịch A. Thêm vào A lượng dư dung dịch BaCl2 loãng, 5,91g kết tủa trắng:
a) Viết phương trình phản ứng xảy ra.
b)Tính thành phần phần trăm theo thể tích của mỗi hidrocacbon trong hỗn hợp ban đầu. Biết rằng nếu cho V lít (đktc) hỗn hợp đó qua lượng dư dung dịch nước brom thì có 3,2g brom tham gia phản ứng.
Câu 5. Một dung dịch Z gồm rượu etylic và nước. Cho 7,44g Z tác dụng với Na dư thấy thoát ra 2,018 lít khí H2 (đo ở đktc). Độ rượu của dung dịch Z là (biết D rượu=0,8g/ml, D nước = 1g/ml)
Đề số 3
Câu 1: (6 điểm)
1 - Cho biết tổng số hạt proton, nơtron, electron trong 2 nguyên tử của nguyên tố A và B là 78, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 26 hạt. Số hạt mang điện của A nhiều hơn số hạt mang điện của B là 28 hạt. Hỏi A, B là nguyên tố gì?
Cho biết điện tích hạt nhân của một số nguyên tố sau: ZN = 7 ; ZNa = 11; ZCa = 20 ; ZFe = 26 ; ZCu = 29 ; ZC = 6 ; ZS = 16.
2 - Hợp chất của A và D khi hoà tan trong nước cho một dung dịch có tính kiềm. Hợp chất của B và D khi hoà tan trong nước cho dung dịch E có tính axit yếu. Hợp chất A, B, D không tan trong nước nhưng tan trong dung dịch E. Xác định hợp chất tạo bởi A và D; B và D; A,B,D. Viết phương trình phản ứng.
3 - Một số nguyên nhân của sự hình thành canxicacbonat trong thạch nhũ ở các hang động đá vôi tuỳ thuộc vào thực tế vì canxihiđrocacbonat là:
a, Chất kết tinh và có thể sủi bọt khí.
b, Có thể tan và không bền.
c, Dễ bay hơi và có thể chảy rữa.
d, Chất kết tinh và không tan.
Câu 2: (4 điểm)
1 - Tìm các chất A,B,C,D,E (hợp chất của Cu) trong sơ đồ sau và viết phương trình hoá học:
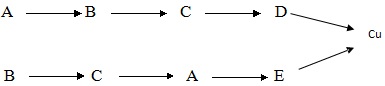
2 - Chỉ dùng thêm nước hãy nhận biết 4 chất rắn: Na2O, Al2O3, Fe2O3, Al chứa trong các lọ riêng biệt. Viết các phương trình phản ứng.
Câu 3: (4 điểm)
Cho 27,4 g Ba vào 400 g dung dịch CuSO4 3,2 % thu được khí A, kết tủa B và dung dịch C.
a, Tính thể tích khí A (đktc).
b, Nung kết tủa B ở nhiệt độ cao đến khối lượng không đổi thì thu được bao nhiêu gam chất rắn?
c, Tính nồng độ phần trăm của chất tan trong dung dịch C.
Câu 4: (6 điểm)
A là hỗn hợp gồm rượu Etylic và 2 axit hữu cơ kế tiếp nhau có dạng CnH2n+1COOH và Cn+1H2n+3COOH. Cho 1/2 hỗn hợp A tác dụng hết với Na thoát ra 3,92 lít H2 (đktc). Đốt 1/2 hỗn hợp A cháy hoàn toàn, sản phẩm cháy được hấp thụ hết vào dung dịch Ba(OH)2 dư thì có 147,75g kết tủa và khối lượng bình Ba(OH)2 tăng 50,1 g.
a, Tìm công thức 2 axit trên .
b, Tìm thành phần hỗn hợp A.
Đề số 4
Câu 1. Hoàn thành sơ đồ bằng phương trình phản ứng:
FeS2 +O2 A↑ + B J
B + D
A + H2S C↓+ D L + B
E + D
C + E F F + HCl
G + H2S↑
G + NaOH H↓+ I H + O2 + D
J↓
Câu 2.
a) Cho các chất: Na, MgCl2, FeCl2, FeCl3, AlCl3 chỉ dùng thêm nước hãy nhận biết chúng
b) Có 3 lọ đựng ba hỗn hợp dạng bột: ( Al + Al2O3), (Fe + Fe2O3) và (FeO + Fe2O3). Dùng phương pháp hóa học để nhận biết chúng. Viết phương trình hoá học xảy ra.
Câu 3. Cho hỗn A gồm 3 oxit: Al2O3, CuO và K2O. Tiến hành 3 thí nghiệm:
Thí nghiệm 1: nếu cho hỗn hợp A vào nước dư, khuấy kĩ thấy còn 15g chất rắn không tan.
Thí nghiệm 2: Nếu cho thêm vào hỗn hợp A một lượng Al2O3 bằng 50% lượng Al2O3 trong A ban đầu rồi lại hòa tan vào nước dư. Sau thí nghiệm còn lại 21g chất rắn không tan.
Thí nghiệm 3: Nếu cho vào hỗn hợp A một lượng Al2O3 bằng 75% lượng Al2O3 trong A, rồi lại hòa tan vào nước dư, thấy còn lại 25g chất rắn không tan.
Tính khối lượng oxit trong hỗn hợp A.
Câu 4. Đốt cháy hết V lít (đktc) hỗn hợp CH4 và C2H4, cho toàn bộ sản phẩm thu được hấp thụ hết vào 100ml dung dịch NaOH 1M, thu được dung dịch A. Thêm vào A lượng dư dung dịch BaCl2 loãng, 5,91g kết tủa trắng:
a) Viết phương trình phản ứng xảy ra.
b)Tính thành phần phần trăm theo thể tích của mỗi hidrocacbon trong hỗn hợp ban đầu. Biết rằng nếu cho V lít (đktc) hỗn hợp đó qua lượng dư dung dịch nước brom thì có 3,2g brom tham gia phản ứng.
Câu 5. Một dung dịch Z gồm rượu etylic và nước. Cho 7,44g Z tác dụng với Na dư thấy thoát ra 2,018 lít khí H2 (đo ở đktc). Độ rượu của dung dịch Z là (biết D rượu = 0,8g/ml, D nước = 1g/ml)
Đề xem đáp án hướng dẫn giải chi tiết bộ đề mời các bạn ấn link TẢI VỀ phía dưới
............................
TimDapAnđã giới thiệu Tuyển tập 30 đề thi học sinh giỏi Hóa học lớp 9 có đáp án đề thi với các dạng bài tập hoàn thành phương trình hóa học, nhận biết các chất, phân tích làm bài tập thí nghiệm, và dạng bài tập tính toán tất cả các dạng này đòi hỏi các em phải hiểu và vận dụng cao để làm đề thi học sinh giỏi Hóa 9.
Trên đây TimDapAnđã giới thiệu Tuyển tập 30 đề thi học sinh giỏi Hóa học lớp 9 tới các bạn. Để có kết quả học tập tốt và hiệu quả hơn, TimDapAnxin giới thiệu tới các bạn học sinh tài liệu Giải bài tập Toán 9, Giải SBT Vật Lí 9, Lý thuyết Sinh học 9, Chuyên đề Hóa học 9. Tài liệu học tập lớp 9 mà TimDapAntổng hợp biên soạn và đăng tải.








