Đề thi học kì 2 Hóa 9 Có đáp án
Bộ đề thi học kì 2 môn Hóa học lớp 9 Có đáp án chi tiết được Tìm Đáp Án sưu tầm và đăng tải là tài liệu ôn tập và hệ thống kiến thức môn Hóa học lớp 9 hiệu quả. Bộ đề thi học kì 2 hóa 9 dưới đây gồm các dạng cấu trúc đề thi hóa 9 cả hình thức đánh giá tự luận và câu hỏi trắc nghiệm khách quan. Đây là tài liệu hay cho các em học sinh ôn luyện trước kì thi. Mời các bạn tải về tham khảo.
Mời các bạn tham khảo đề thi hóa 9 học kì 2 mới nhất do TimDapAnbiên soạn này
Đề kiểm tra hóa 9 học kì 2 - Đề Số 1
I. TRẮC NGHIỆM KHÁCH QUAN
Câu 1: Benzen làm mất màu dung dịch brom vì:
A. Phân tử benzen là chất lỏng có cấu tạo vòng.
B. Phân tử benzen là chất lỏng có cấu tạo vòng và có 3 liên kết đôi.
C. Phân tử benzen có 3 liên kết đôi xen kẽ 3 liên kết đơn.
D. Phân tử benzen có cấu tạo vòng trong đó có 3 liên kết đôi xen kẽ 3 liên kết đơn.
Câu 2: Hiđrocacbon nào sau đây phản ứng cộng với dung dịch Brom?
A. CH3-CH2-CH3.
B. CH3-CH3.
C. C2H4
D. CH4.
Câu 3: Khi đốt cháy hoàn toàn 2 mol khí butan C4H10 cần ít nhất là:
A. 6.5mol khí O2
B. 13 mol khí O2.
C. 12 mol khí O2
C. 10 mol khí O2..
Câu 4: Khí ẩm nào sau đây có tính tẩy màu?
A. CO.
B. Cl2.
C. CO2
D. H2.
Câu 5: Dãy các nguyên tố được sắp xếp theo chiều tính phi kim tăng dần là:
A. Cl, Si, S, P.
B. Cl, Si, P, S.
C. Si, S, P, Cl.
D. S i, P, S, Cl.
Câu 6: Dẫn 1 mol khí axetilen vào dung dịch chứa 4 mol brom. Hiện tượng quan sát là:
A. màu da cam của dung dịch brom nhạt hơn so với ban đầu.
B. màu da cam của dung dịch brom đậm hơn so với ban đầu.
C. màu da cam của dung dịch brom trở thành không màu.
D. không có hiện tượng gì xảy ra.
Câu 7: Đốt cháy hoàn toàn 1.17g hợp chất hữu cơ A thu được 2.016 lít CO2 đktc và 0.81 g H2O.Biết rằng số mol của A bằng số mol của 0.336 lít H2. Công thức phân tử A là:
A. CH4.
B. C2H4.
C. C2H6O.
D. C6H6.
Câu 8: Dãy chất nào sau đây đều phản ứng với dung dịch NaOH?
A. CH3COOH, C2H5OH.
B. CH3COOH, C6H12O6.
C. CH4, CH3COOC2H5.
D. CH3COOC2H5.
Câu 9: Dung dịch nào sau đây không thể chứa trong bình thủy tinh.
A. HNO3
B. HCl
C. H2SO4.
D. HF.
Câu 10: Số ml rượu etylic có trong 250 ml rượu 45 độ là:
A. 250ml
B. 215ml
C. 112.5ml
D. 75ml.
II. Tự luận: 7 điểm
Câu 1: Có 4 chất sau: NaHCO3, KOH, CaCl2, CaCO3.
a/ Chất nào tác dụng với dung dịch HCl?
b/ Chất nào tác dụng với NaOH? Viết phương trình hóa học xảy ra?.
Câu 2: Trình bày phương pháp hóa học để nhận biết các khí sau đây: C6H6, C2H4, H2. Viết phương trình phản ứng xảy ra nếu có?
Câu 3: Chia a g axít axetic thành 2 phần bằng nhau.
Phần 1 trung hòa vừa đủ với 0.25 lít dd NaOH 0.25lít dd NaOH 0.2M.
Phần 2 thực hiện phản ứng este hóa với rượu etylic thu được m g este giả sử hiệu suất xảy ra hoàn toàn.
a/ Viết phương trình phản ứng xảy ra?
b/ Tính giá trị của a và m?
Đáp án đề kiểm tra học kì 2 hóa 9 Đề số 1
Phần 1. Trắc nghiệm khách quan
| 1D | 2B | 3B | 4B | 5D |
| 6C | 7D | 8D | 9D | 10C |
Phần 2. Tự luận
Câu 1
a)
NaHCO3 + HCl → NaCl + CO2 + H2O
KOH + HCl → CaCl2 + 2H2O
CaCO3 + 2HCl → CaCl2 + CO2 + H2O
b)
NaHCO3 + NaOH → Na2CO3 + H2O
Câu 2
Dẫn các khí đi qua Br2 dư, khí nào làm dd Br2 mất màu là C2H4:
C2H4 + Br2 → C2HBr2
Còn lại C2H6 và H2.
Dẫn 2 khí đi qua bột CuO nung nóng.
Khí nào làm bột đồng chuyển đỏ là H2: H2 + CuO → Cu + H2O
Còn lại là C2H6
Câu 3.
Phương trình phản ứng hóa học
CH3COOH + NaOH → CH3COONa + H2O
0,05 ← 0,05
CH3COOH + C2H5OH → CH3COOC2H5 + H2O
0,05 ← 0,05
Tổng số mol CH3COOH = 0,05 + 0,05 = 0,1 mol
a = 0,1.60 = 6 g
m = 0,05.88 = 4,4g
Đề kiểm tra hóa 9 học kì 2 - Đề số 2
I. Trắc nghiệm khách quan: (15 phút)
Hãy khoanh tròn vào một trong các chữ cái A, B, C hoặc D đứng trước câu trả lời đúng nhất.
Câu 1: Những hiđrôcacbon nào sau đây trong phân tử chỉ có liên kết đơn:
A. Etylen.
B. Benzen.
C. Metan.
D. Axetylen.
Câu 2: Một hiđrôcacbon thành phần chứa 75% Cacbon, Hy đrôcacbon có công thức hóa học:
A. C2H2
B. C2H4
C. C3H6
D. CH4
Câu 3: Giấm ăn là dung dịch A xit a xê tic có nồng độ:
A. 2—5 %
B. 10—20%
C. 20—30%
D. Một kết quả khác
Câu 4: Thể tích rượu êtylíc nguyên chất có trong 500ml rượu 20 độ là:
A. 100ml
B. 150ml
C. 200ml
D. 250ml
Câu 5: Những hidrocacbon nào sau đây trong phân tử vừa có liên kết đơn, vừa có liên kết ba.
A. Etylen
B. Benzen
C. Metan
D. Axetylen
Câu 6: Rượu êtylic phản ứng được với Natri vì:
A. Trong phân tử có nguyên tử H và O.
B. Trong phân tử có nguyên tử C, H và O.
C. Trong phân tử có nhóm –OH.
C. Trong phân tử có nguyên tử ôxi.
Câu 7: Dầu ăn là:
A. Este của glixerol.
B. Este của glixerol và axít béo
C. Este của axit axetic với glixerol
D. Hỗn hợp nhiều este của glixerol và các axit béo
Câu 8: Có 2 bình đựng khí khác nhau là CH4 và CO2. Để phân biệt các chất ta có thể dùng :
A. Một kim loại
B. Dung dịch Ca(OH)2
C. Nước Brôm
D. Tất cả đều sai
Câu 9: Tính chất nào sau đây không phải là của khí Clo:
A. Tan hoàn toàn trong nước
B. Có màu vàng lục
C. Có tính tẩy trắng khi ẩm
D. Có mùi hắc, rất độc
Câu 10: Những dãy chất nào sau đây đều là Hiđrocacbon :
A. FeCl2, C2H6O, CH4, NaHCO3
B. C6H5ONa, CH4O, HNO3, C6H6
C. CH4, C2H4, C2H2, C6H6
D. CH3NO2, CH3Br, NaOH
Câu 11: Chỉ dùng quỳ tím và kim loại Na có thể phân biệt 3 dung dịch nào sau đây :
A. HCl, CH3COOH, C2H5OH.
B. CH3COOH, C2H5OH, H2O.
C. CH3COOH, C2H5OH, C6H6
D. C2H5OH , H2O, NaOH.
Câu 12: Trong các chất sau, chất nào có phản ứng tráng bạc:
A. Xenlulôzơ.
B. Glucozơ.
C. Protêin.
D. Tinh bột.
II.Phần tự luận:( 7 điểm)
Câu 1: ( 2 điểm) Viết phương trình hoá học thực hiện các chuyển đổI hoá học theo sơ đồ sau:
C2H4 → C2H5OH → CH3COOH →CH3COOC2H5 → CH3COONa
Câu 2: (2 điểm): Trình bày phương pháp hóa học nhận biết 3 lọ bị mất nhãn: rượu etylic, axitaxetic, benzen.
Câu 3: (2 điểm) Đốt cháy hoàn toàn 6,4g chất hữu cơ A, thu được 8,8g khí CO2 và 7,2 g H2O. Biết tỉ khối hơi của A so với H2 là 16. Tìm công thức phân tử của A và viết công thức cấu tạo của A
Đáp án đề kiểm tra hóa 9 học kì 2 Đề số 2
Phần 1. Trắc nghiệm khách quan
| 1C | 2D | 3A | 4A | 5D | 6C |
| 7D | 8B | 9A | 10C | 11C | 12B |
Phần 2. Tự luận
Câu 1.
C2H4 + H2O → C2H5OH
C2H5OH + O2 CH3COOH + H2O
CH3COOH + C2H5OH → CH3COOC2H5 + H2O
CH3COOC2H5 + NaOH → CH3COONa + C2H5OH
Câu 2.
Trích mẫu thử và đánh số thứ tự
Dùng quỳ tím nhận được axit axetic (quì tím hóa đỏ)
Cho mẫu kim loại Na vào hai mẫu còn lại, nếu mẫu thử nào có sủi bọt khí H2 là rượu etylic
C2H5OH + Na → C2H5ONa + 1/2H2 (khí)
Mẫu thử còn lại không có hiện tượng gì là benzen.
Câu 3.
nCO2= 0,2 = nC => mC = 2,4g
nH = 2nH2O = 0,8 mol => mH = 0,8g
Bảo toàn nguyên tố Oxi
=> mO = 6,4 - 2,4 - 0,8 = 3,2g
=> nO = 0,2 mol
nC: nH : nO= 0,2: 0,8: 0,2= 1:4:1
=> CTĐGN (CH4O)n
M= 16 .2 = 32 => n=1
Vây CTPT là CH4O
Đề kiểm tra hóa 9 học kì 2 - Đề số 3
Phần 1: Trắc nghiệm (4 điểm)
Chọn và khoanh tròn vào chữ cái đứng trước phương án trả lời đúng
Câu 1. Etilen thuộc nhóm
A. Hidrocacbon
B. Dẫn xuất hidrocacbon
C. Chất rắn
D. Chất lỏng
Câu 2. Phát biểu nào sau đúng khi nói về metan?
A. Khí metan có nhiều trong thành phần khí quyển trái đất.
B. Trong cấu tạo phân tử metan có chứa liên kết đôi.
C. Metan cháy tạo thành khí CO2 và H2O.
D. Metan là nguồn nguyên liệu để tổng hợp nhựa PE trong công nghiệp.
Câu 3. Số công thức cấu tạo mạch hở của C4H8 là:
A. 1
B. 2
C. 3
D. 4
Câu 4. Gluxit nào sau đây có phản ứng tráng gương?
A. Tinh bột.
B. Glucozơ.
C. Xenlulozơ.
D. Saccarozo.
Câu 5. Ancol etylic tác dụng được với
A. Na
B. Al
C. Fe
D. Cu
Câu 6. Hidrocacbon A là chất có tác dụng kích thích trái cây mau chín. A là chất nào trong các chất dưới đây?
A. Etilen
B. Bezen
C. Metan
D. Axetilen
Câu 7. Glucozơ có tính chất nào dưới đây?
A. Làm đổi màu quỳ tím.
B. Tác dụng với dung dịch axit.
C. Phản ứng thủy phân.
D. Phản ứng với dung dịch AgNO3 trong NH3.
Câu 8. Nhận xét nào dưới đây là đúng khi nói về polime?
A. Đa số các polime dễ hòa tan trong các dung môi thông thường.
B. Các polime có phân tử khối rất lớn.
C. Các polime dễ bay hơi.
D. Đa số các polime không có nhiệt độ nóng chảy xác định.
Câu 9. Thể tích oxi (đktc) cần thiết đốt cháy 4,6 gam ancol etylic là:
A. 6,72 lít
B. 7,84 lít
C. 8.69 lít
D. 11,2 lít
Câu 10. Thủy phân protein trong dung dịch axit sinh ra sản phẩm là:
A. Ancol etylic.
B. Axit axetic.
C. Grixerol.
D. Amino axit.
Phần 2. Tự luận (6 điểm)
Câu 1. (2 điểm) Viết phương trình hóa học thực hiện sơ đồ chuyển đối hóa học sau:
Glucozơ → Rượu etylic → Axit axetic → Natri axetat → Metan
Câu 2. (1,5 điểm) Nhận biết các chất dưới đây bằng phương pháp hóa học:
Acol etylic, axit axetic, glucozơ
Câu 3. (2,5 điểm) Đốt cháy hoàn toàn 4,8 gam một hợp chất hữu cơ A sau phản ứng thu được 6,6 gam CO2 và 5,4 gam H2O. Biết rằng khi hóa hơi ở điều kiện tiêu chuẩn 2,24 lít khí A nặng 3,2 gam.
a) Xác định công thức phân tử của hợp chất hữu cơ A.
b) Biết rằng A có phản ứng với Na. Tính thể tích khí hidro (đktc) thoát ra khi cho lượng chất A ở trên phản ứng hoàn toàn với Na dư.
(Na = 23, O = 16, C = 16, H = 1)
Đáp án đề thi học kì 2 hóa 9 Đề số 3
Phần 1. Trắc nghiệm khách quan
| 1A | 2C | 3C | 4B | 5A |
| 6A | 7D | 8D | 9A | 10D |
Phần 2. Tự luận
Câu 1.
(1) C6H12O6 → 2C2H5OH + CO2
(2) C2H5OH + O2 → CH3COOH + H2O
(3) CH3COOH + NaOH → CH3COONa + H2O
(4) CH3COONa + NaOH → CH4 + Na2CO3
Câu 2.
Nhúng quỳ tím vào các chất trên, chất làm đổi màu quỳ tím thành đỏ là axit axetic. Các chất còn lại không làm đổi màu quỳ tím.
Nhỏ dung dịch AgNO3/NH3 vào các chất còn lại, chất nào xảy ra phản ứng tráng gương là glucozơ.
C6H12O6 + Ag2O → C6H12O7 + 2Ag ↓
Ancol etylic không phản ứng với AgNO3/NH3
Câu 3.
a) nCO2 = 0,15 mol
A phản ứng với Na => A có nhóm -OH: CH3OH
Đề kiểm tra hóa 9 học kì 2 - Đề số 4
Phần 1: Trắc nghiệm (4 điểm)
Chọn và khoanh tròn vào chữ cái đứng trước phương án trả lời đúng
Câu 1. Etilen thuộc nhóm
A. Hidrocacbon
B. Dẫn xuất hidrocacbon
C. Chất rắn
D. Chất lỏng
Câu 2. Phát biểu nào sau đúng khi nói về metan?
A. Khí metan có nhiều trong thành phần khí quyển trái đất.
B. Trong cấu tạo phân tử metan có chứa liên kết đôi.
C. Metan cháy tạo thành khí CO2 và H2O.
D. Metan là nguồn nguyên liệu để tổng hợp nhựa PE trong công nghiệp.
Câu 3. Số công thức cấu tạo mạch hở của C4H8 là:
A. 1
B. 2
C. 3
D. 4
Câu 4. Gluxit nào sau đây có phản ứng tráng gương?
A. Tinh bột.
B. Glucozơ.
C. Xenlulozơ.
D. Saccarozo.
Câu 5. Ancol etylic tác dụng được với
A. Na
B. Al
C. Fe
D. Cu
Câu 6. Hidrocacbon A là chất có tác dụng kích thích trái cây mau chín. A là chất nào trong các chất dưới đây?
A. Etilen
B. Bezen
C. Metan
D. Axetilen
Câu 7. Glucozơ có tính chất nào dưới đây?
A. Làm đổi màu quỳ tím.
B. Tác dụng với dung dịch axit.
C. Phản ứng thủy phân.
D. Phản ứng với dung dịch AgNO3 trong NH3.
Câu 8. Nhận xét nào dưới đây là đúng khi nói về polime?
A. Đa số các polime dễ hòa tan trong các dung môi thông thường.
B. Các polime có phân tử khối rất lớn.
C. Các polime dễ bay hơi.
D. Đa số các polime không có nhiệt độ nóng chảy xác định.
Câu 9. Thể tích oxi (đktc) cần thiết đốt cháy 4,6 gam ancol etylic là:
A. 6,72 lít
B. 7,84 lít C. 8.69 lít D. 11,2 lít
Câu 10. Thủy phân protein trong dung dịch axit sinh ra sản phẩm là:
A. Ancol etylic. B. Axit axetic. C. Grixerol. D. Amino axit.
Phần 2. Tự luận (6 điểm)
Câu 1. (2 điểm) Viết phương trình hóa học thực hiện sơ đồ chuyển đối hóa học sau:
Glucozơ Rượu etylic Axit axetic Natri axetat Metan
Câu 2. (1,5 điểm) Nhận biết các chất dưới đây bằng phương pháp hóa học:
Acol etylic, axit axetic, glucozơ
Câu 3. (2,5 điểm) Đốt cháy hoàn toàn 4,8 gam một hợp chất hữu cơ A sau phản ứng thu được 6,6 gam CO2 và 5,4 gam H2O. Biết rằng khi hóa hơi ở điều kiện tiêu chuẩn 2,24 lít khí A nặng 3,2 gam.
a) Xác định công thức phân tử của hợp chất hữu cơ A.
b) Biết rằng A có phản ứng với Na. Tính thể tích khí hidro (đktc) thoát ra khi cho lượng chất A ở trên phản ứng hoàn toàn với Na dư.
(Na = 23, O = 16, C = 16, H = 1)
Đáp án đề thi học kì 2 hóa 9 Đề số 4
Phần 1. Trắc nghiệm(2 điểm)
| 1A | 2C | 3C | 4B | 5A |
| 6A | 7D | 8B | 9A | 10D |
Phần 2. Tự luận (6 điểm)
Câu 1.
(1) C6H12O6 2C2H5OH + CO2
(2) C2H5OH + O2 CH3COOH + H2O
(3) CH3COOH + NaOH →CH3COONa + H2O
(4) CH3COONa + NaOH CH4 + Na2CO3
Câu 2.
Nhúng quỳ tím vào các chất trên, chất làm đổi màu quỳ tím thành đỏ là axit axetic. Các chất còn lại không làm đổi màu quỳ tím.
Nhỏ dung dịch AgNO3/NH3 vào các chất còn lại, chất nào xảy ra phản ứng tráng gương là glucozơ.
C6H12O6 + Ag2O C6H12O7 + 2Ag ↓
Ancol etylic không phản ứng với AgNO3/NH3
Câu 3.
a) nCO2 = 0,15 mol
b) nH2O = 0,3 mol
c)
d) A phản ứng với Na =>A có nhóm -OH: CH3OH
Đề kiểm tra hóa 9 học kì 2 - Đề số 5
Phần 1: Trắc nghiệm (4 điểm)
Chọn và khoanh tròn vào chữ cái đứng trước phương án trả lời đúng
Câu 1. Trong phân tử metan có
A. 4 liên kết đơn C-H
B. 1 liên kết đôi C=H và 3 liên kết đơn C-H
C. 2 liên kết đôi C=O và 2 liên kết đơn C-H
D. 1 liên kết đôi C=H và 3 liên kết đơn C-H
Câu 2. Đốt cháy 1 hydrocacbon được nH2O gấp đôi nCO2. Tìm công thức hydrocacbon đó là:
A.C2H6
B. CH4
C. C2H4
D. C2H2
Câu 3. Số công thức cấu tạo mạch hở của rượu có công thức C4H8O là:
A. 2
B. 3
C. 4
D. 5
Câu 4. Chọn câu trả lời đúng trong các câu trả lời sau:
CH4làm mất mất màu dung dịch brom
C2H4tham gia phản ứng thế với clo tương tư như CH4
CH4và C2H4 đều tham gia phản ứng cháy sinh ra CO2 và H2O
CH4và CO2 đều có phản ứng trùng hợp
Câu 5.Hợp chất Y là chất lỏng không màu, có nhóm – OH trong phân tử, tác dụng với kali nhưng không tác dụng với kẽm. Y là
A. NaOH.
B. CH3COOH.
C. Ca(OH)2.
D. C2H5OH.
Câu 6. Dãy chất tác dụng với axit axetic là:
A. CuO; Cu(OH)2; Cu; CuSO4; C2H5
B. CuO; Cu(OH)2; Zn ; H2SO4; C2H5
C. CuO; Cu(OH)2; Zn ; Na2CO3;C2H5
D. CuO; Cu(OH)2; C2H5OH; C6H6; CaCO3.
Câu 7. Cho sơ đồ sau:
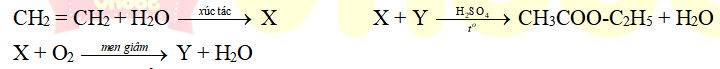
Vậy X, Y có thể là:
C2H6, C2H5
C2H5OH, CH3
C2H5OH, CH3
C2H4, C2H5OH.
Câu 8. Cặp chất tồn tại được trong một dung dịch là (không xảy ra phản ứng hóa học với nhau)
CH3COOH và NaOH.
CH3COOH và H3PO4.
CH3COOH và Ca(OH)2.
CH3COOH và Na2CO3.
Câu 9. Thủy phân chất béo trong môi trường axit thu được
A. glixerol và một số loại axit béo.
B. glixerol và một loại axit béo.
C. glixerol và một muối của axit béo.
D. glixerol và xà phòng
Câu 10. Aminoaxit (A) chứa 13,59% nitơ về khối lượng. Công thức phân tử của aminoaxit là
A. C3H7O2N.
B. C4H9O2N.
C. C5H11O2N.
D. C6H13O2N.
Phần 2. Tự luận (6 điểm)
Câu 1. (2 điểm) Viết phương trình hóa học thực hiện sơ đồ chuyển đối hóa học sau:
![]()
Câu 2. (2 điểm) Bằng phương pháp hóa học hãy phân biệt các chất sau: C2H5OH, C6H12O6, C12H22O11 .
Câu 3. (2 điểm) Hỗn hợp A gồm metan và etilen. Đốt cháy hoàn toàn 2,24 lít hỗn hợp A (đktc) rồi cho sản phẩm đi qua bình đựng dung dịch Ba(OH)2 dư tạo ra 27,58 gam kết tủa.
a. Viết phương trình hóa học?
b. Tính thành phần, phần trăm thể tích hỗn hợp ban đầu
Xem đáp án trong file tải
Tài liệu vẫn còn dài, mời các bạn tải miễn phí các đề này về qua đường link bên dưới để ôn thi tốt hơn
...................................................
TimDapAnđã gửi tới các bạn bộ tài liệu Bộ đề thi học kì 2 môn Hóa học lớp 9 Có đáp án chi tiết tới các bạn. Để có kết quả cao hơn trong học tập, TimDapAnxin giới thiệu tới các bạn học sinh tài liệu Giải bài tập Hóa học 9 mà TimDapAntổng hợp và đăng tải để học tốt Hóa học 9.
Ngoài ra, để chuẩn bị cho kì thi học kì 2 lớp 9 sắp tới đạt kết quả cao, các em học sinh cần thực hành luyện đề để nâng cao kỹ năng giải đề cũng như làm quen với nhiều dạng đề thi khác nhau. Chuyên mục Đề thi học kì 2 lớp 9 nói chung và Đề thi học kì 2 lớp 9 môn Hóa nói riêng, sẽ là nguồn tài liệu phong phú và hữu ích cho các em ôn tập, củng cố kiến thức, ôn luyện hiệu quả.
Ngoài ra, Tìm Đáp Án đã thành lập group chia sẻ tài liệu học tập THCS miễn phí trên Facebook: Luyện thi lớp 9 lên lớp 10. Mời các bạn học sinh tham gia nhóm, để có thể nhận được những tài liệu mới nhất.








