Đề thi thử THPT Quốc gia 2017 môn Hóa học
Mời các bạn học sinh cùng tham khảo: Đề thi thử THPT Quốc gia năm 2017 môn Hóa học trường THPT Thực hành Cao Nguyên, Đăk Lăk (Lần 2) để làm quen với cấu trúc đề thi, các dạng bài tập thường ra trong kì thi THPT Quốc gia. Chúc các bạn ôn thi tốt và đạt được kết quả cao.
Đề thi thử THPT Quốc gia năm 2017 môn Hóa học Sở GD&ĐT Lâm Đồng
Đề thi thử THPT Quốc gia năm 2017 môn Hóa học Sở GD&ĐT Bắc Giang
| TRƯỜNG ĐẠI HỌC TÂY NGUYÊN ĐỀ THI CHÍNH THỨC | ĐỀ THI THỬ THPT QUỐC GIA 2017 (LẦN 2) Bài thi: KHOA HỌC TỰ NHIÊN Môn thi thành phần: HÓA Thời gian làm bài: 50 phút (không kể thời gian giao đề) (Đề thi có 04 trang - 40 câu trắc nghiệm) Mã đề thi: 132 |
Cho biết nguyên tử khối của các nguyên tố: H = 1; C = 12; N = 14; O = 16; Na = 23; Mg = 24; Al = 27; S = 32; Cl = 35,5; K = 39; Ca = 40; Mn = 55; Fe = 56; Cu = 64; Zn = 65; Br = 80; Ag = 108; Ba = 137; P = 31; Mn = 55
Câu 41: Mệnh đề không đúng là:
A. CH3CH2COOCH=CH2 tác dụng được với dung dịch Br2.
B. CH3CH2COOCH=CH2 có thể trùng hợp tạo polime.
C. CH3CH2COOCH=CH2 tác dụng với dung dịch NaOH thu được anđehit và muối.
D. CH3CH2COOCH=CH2 cùng dãy đồng đẳng với CH2=CHCOOCH3
Câu 42: Kim loại chỉ được điều chế bằng phương pháp điện phân nóng chảy là
A. Cu B. Fe C. Ag D. K
Câu 43: Tên thay thế của amino axit có công thức cấu tạo CH3−CH(CH3)−CH(NH2)−COOH
A. Axit α – aminoisovaleric. B. Axit 2 – amino – 3 -metylbutanoic.
C. Axit 2 – aminoisopentanoic. D. Axit α – aminoisovaleric.
Câu 44: Một dung dịch X có các tính chất:
- Tác dụng Cu(OH)2 cho phức màu xanh lam.
- Tác dụng dung dịch [Ag(NH3)2]OH.
- Bị thuỷ phân khi có mặt xúc tác axit hoặc enzim.
Dung dịch X là:
A. Fructozơ B. Saccarozơ C. Glucozơ D. Mantozơ.
Câu 45: Kim loại M có các tính chất: nhẹ, bền trong không khí ở nhiệt độ thường; tan được trong dung dịch NaOH nhưng không tan trong dung dịch HNO3 đặc nguội và H2SO4 đặc nguội. Kim loại M là:
A. Al B. Fe C. Cr D. Zn
Câu 46: Polime thiên nhiên X được sinh ra trong quá trình quang hợp của cây xanh. Tiến hành thí nghiệm: Nhỏ vài giọt nước clo vào dung dịch chứa Natri iotua, sau đó cho polime X tác dụng với dung dịch thu được thấy tạo màu xanh tím. Polime X là
A. tinh bột. B. xenlulozơ. C. saccarozơ. D. glicogen.
Câu 47: Phát biểu nào sau đây chưa chính xác
A. Glucozơ là hợp chất hữu cơ tạp chức.
B. Metylamin là chất lỏng ở điều kiện thường, làm quỳ tím hóa xanh.
C. Etyl fomat cho được phản ứng tráng gương.
D. Amino axit là chất rắn ở điều kiện thường và dễ tan trong nước.
Câu 48: Cho một số tính chất: có dạng sợi (1); tan trong nước (2); tan trong nước Svayde (3); phản ứng với axit nitric đặc (xúc tác axit sunfuric đặc) (4); tham gia phản ứng tráng bạc (5); bị thuỷ phân trong dung dịch axit đun nóng (6). Các tính chất của xenlulozơ là:
A. (2), (3), (4) và (5). B. (3), (4), (5) và (6). C. (1), (2), (3) và (4). D. (1), (3), (4) và (6)
Câu 49: Nước cứng là nước chứa nhiều các ion:
A. Cu2+, Fe3+ B. Al3+, Fe3+ C. Na+, K+ D. Ca2+, Mg2+
Câu 50: Chất thơm P thuộc loại este có công thức phân tử C8H8O2. Chất P không được điều chế từ phản ứng của axit và ancol tương ứng, đồng thời không có khả năng phản ứng tráng gương. Công thức cấu tạo thu gọn của P là công thức nào
A. H-COO-C6H4-CH3 B. C6H5-COO-CH3
C. H-COO- CH2 - C6H5 D. CH3COO-C6H5
Câu 51: Cấu hình của ion Fe3+ là
A. 1s22s22p63s23p63d64s2 B. 1s22s22p63s23p63d64s1
C. 1s22s22p63s23p63d6 D. 1s22s22p63s23p63d5
Câu 52: Mô tả nào dưới đây không phù hợp với nhôm (Z=13)
A. Cấu hình electron [Ne] 3s23p1
B. Là một kim loại lưỡng tính.
C. Mức oxi hóa đặc trưng + 3.
D. Ở ô 13, chu kì 3, nhóm IIIA.
Câu 53: Số đồng phân bậc một của amin có công thức phân tử C4H11N là
A. 6. B. 3 C. 5. D. 4
Câu 54: Để trung hòa 20 ml dung dịch HCl 0,1M cần 10 ml dung dịch NaOH nồng độ x mol/l. Giá trị của x là
A. 0,4 B. 0,3 C. 0,2 D. 0,1
Câu 55: Hòa tan hoàn toàn 20 gam hỗn hợp Mg và Fe bằng dung dịch HCl dư. Sau phản ứng thu được 11,2 lít khí (đktc) và dung dịch X. Cô cạn dung dịch X thì thu được bao nhiêu gam muối khan
A. 90,0 gam. B. 71,0 gam. C. 91,0 gam. D. 55,5 gam.
Câu 56: Hỗn hợp A gồm 3 kim loại: Cu, X, Fe. Để tách rời kim loại X ra khỏi hỗn hợp A mà không làm thay đổi khối lượng X, dùng 1 hóa chất duy nhất là muối nitrat sắt. Kim loại X là
A. Al. B. Ag. C. Zn. D. Pb.
Câu 57: Khi thêm dung dịch Na2CO3 vào dung dịch FeCl3 sẽ có hiện tượng gì xảy ra?
A. Xuất hiện kết tủa màu nâu đỏ vì xảy ra hiện tượng thủy phân.
B. Xuất hiện kết tủa màu nâu đỏ đồng thời có hiện tượng sủi bọt khí.
C. Dung dịch vẫn có màu nâu đỏ vì chúng không pứ với nhau.
D. Có kết tủa nâu đỏ tạo thành sau đó tan lại do tạo khí CO2.
Câu 58: Ứng dụng không hợp lí của crom là
A. Crom là kim loại rất cứng có thể dùng cắt thủy tinh.
B. Crom làm hợp kim cứng và chịu nhiệt hơn, nên dùng để tạo thép cứng, không gỉ, chịu nhiệt.
C. Crom là kim loại nhẹ, nên được sử dụng tạo các hợp kim dùng trong ngành hàng không.
D. Điều kiện thường, crom tạo được lớp màng oxit mịn, bền chắc nên được dùng để mạ bảo vệ thép.
Câu 59: Trường hợp nào sau đây nước được coi là không bị ô nhiễm
A. Nước sinh hoạt từ nhà máy nước hoặc nước giếng khoan không chứa các độc tố như asen, sắt ... quá mức cho phép.
B. Nước ruộng có chứa khoảng 1% thuốc trừ sâu và phân bón hóa học.
C. Nước thải từ các bệnh viện, khu vệ sinh chứa vi khuẩn gây bệnh.
D. Nước thải từ các nhà máy có chứa nồng độ lớn các ion kim loại nặng như Pb2+, Cd2+, Hg2+, Ni2+
Câu 60: Dung dịch sau đây không hoà tan được đồng kim loại (Cu) là
A. Dung dịch FeCl3. B. Dung dịch HCl loãng.
C. Dung dịch hỗn hợp NaNO3 và HCl. D. Dung dịch axit HNO3.
Câu 61: Hai dây phơi làm bằng hai kim loại nguyên chất là Cu và Al, được nối với nhau rồi để trong không khí ẩm. Chỗ nối của 2 dây kim loại có thể xảy ra hiện tượng nào sau đây
A. Xảy ra hiện tượng ăn mòn điện hóa, Cu là cực dương và bị ăn mòn
B. Xảy ra hiện tượng ăn mòn điện hóa, Cu là cực âm và bị ăn mòn
C. Xảy ra hiện tượng ăn mòn điện hóa, Al là cực dương và bị ăn mòn
D. Xảy ra hiện tượng ăn mòn điện hóa, Al là cực âm và bị ăn mòn
Câu 62: Cho este có công thức phân tử là C4H6O2 khi thủy phân cho ancol metylic thì tên gọi của axit tương ứng của nó là
A. Axit acrylic. B. Axit propionic. C. Axit oxalic D. Axit axetic
Câu 63: Đốt cháy hoàn toàn 0,1 mol một amin no, mạch hở X bằng oxi vừa đủ thu được 0,5 mol hỗn hợp Y gồm khí và hơi. Cho 4,6g X tác dụng với dung dịch HCl (dư), số mol HCl phản ứng là
A. 0,1 B. 0,4 C. 0,3 D. 0,2
Câu 64: Cho x mol Fe tan hoàn toàn trong dung dịch chứa y mol H2SO4 (tỷ lệ x:y = 2:5), thu được một sản phẩm khử duy nhất và dung dịch chỉ chứa muối sunfat. Số mol electron do lượng Fe trên nhường khi bị hòa tan là
A. 3x. B. y. C. 2x. D. 2y.
Câu 65: Cho 49,28lít (đktc) hỗn hợp khí X gồm CO, CO2, N2 có tổng khối lượng là 64,8 gam đi qua 200ml dung dịch chứa NaOH 0,4M và Ba(OH)2 0,4M. Sau khi các phản ứng xảy ra hoàn toàn thu được m gam kết tủa. Giá trị của m là
A. 39,4. B. 19,70. C. 7,88. D. 15,76.
Câu 66: Cho m gam bột Fe vào 200 ml dung dịch hỗn hợp A chứa H2SO4 1M, Fe(NO3)3 0,5M và CuSO4 0,25M. Khuấy đều cho đến khi phản ứng kết thúc thu được 0,75m gam chất rắn. Giá trị của m là
A. 43,2 gam B. 56 gam C. 33,6 gam D. 32 gam
Câu 67: Trong các phát biểu sau, có bao nhiêu phát biểu đúng
(a) Nhôm vừa tan trong dd HCl, vừa tan trong dd NaOH
(b) Quặng chứa nhiều sắt nhất là hematit.
(c) Điện phân nước, người ta thu được khí oxi ở catot.
(d) CaSO4 là thạch cao sống.
(e) Trong công nghiệp, người ta điều chế Al bằng cách điện phân nóng chảy nhôm oxit.
(f) Độ dẫn điện của Cu lớn hơn Al
A. 4 B. 3 C. 5 D. 6
Câu 68: Thực hiện các thí nghiệm sau:
(a) Nhiệt phân AgNO3 (b) Nung FeS2 trong không khí
(c) Nhiệt phân KNO3 (d) Nhiệt phân Cu(NO3)2
(e) Cho Fe vào dd CuSO4 (g) Cho Zn vào dd FeCl3 (dư)
(h) Nung Ag2S trong không khí (i) Cho Ba vào dd CuSO4 (dư)
Số thí nghiệm thu được kim loại sau khi các phản ứng kết thúc là:
A. 4 B. 3 C. 5 D. 2
Câu 69: Hỗn hợp bột X gồm Cu, Zn. Đốt cháy hoàn toàn m gam X trong oxi (dư), thu được 40,3 gam hỗn hợp gồm CuO và ZnO. Mặt khác, nếu cho 0,25 mol X phản ứng với một lượng dư dung dịch KOH loãng nóng, thì thu được 3,36 lít khí H2 (đktc). Phần trăm khối lượng của Cu trong X là
A. 29,72%. B. 59,44%. C. 19,81%. D. 39,63%.
Câu 70: Xà phòng hóa hoàn toàn 66,6 gam hỗn hợp hai este HCOOC2H5 và CH3COOCH3 bằng dung dịch NaOH, thu được hỗn hợp X gồm hai ancol. Đun nóng hỗn hợp X với H2SO4 đặc ở 1400C, sau khi phản ứng xảy ra hoàn toàn thu được m gam nước. Giá trị của m là
A. 8,10. B. 18,00. C. 16,20. D. 4,05.
Câu 71: Cho hình vẽ mô tả thí nghiệm điều chế khí Z từ dung dịch X và chất rắn Y Hình vẽ bên minh họa cho phản ứng nào sau đây?
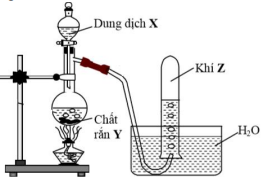
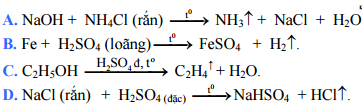
Câu 72: Thủy phân hỗn hợp gồm 0,02 mol saccarozơ và 0,03 mol mantozơ trong môi trường axit, với hiệu suất 60% theo mỗi chất, thu được dung dịch X. Trung hòa dung dịch X, thu được dung dịch Y, sau đó cho toàn bộ Y tác dụng với lượng dư dung dịch AgNO3/NH3, thu được m gam Ag. Giá trị m là:
A. 10,8 gam B. 12,096 gam C. 15,552 gam D. 10,368 gam
Câu 73: Cho các phát biểu sau:
(1) Ở điều kiện thường, anilin là chất rắn, tan ít trong nước.
(2) Nhỏ nước brom vào dung dịch anilin, thấy xuất hiện kết tủa trắng.
(3) Dung dịch anilin làm phenolphtalein đổi màu.
(4) Ứng với công thức phân tử C2H7N, có số đồng phân amin bậc 2 là 1.
(5) Các peptit đều cho phản ứng màu biure.
Tổng số phát biểu đúng là
A. 3. B. 5 C. 2. D. 4
Câu 74: Cho 7,65 gam hỗn hợp X gồm Al và Al2O3 (trong đó Al chiếm 60% khối lượng) tan hoàn toàn trong dung dịch Y gồm H2SO4 và NaNO3, thu được dung dịch Z chỉ chứa 3 muối trung hòa và m gam hỗn hợp khí T (trong T có 0,015 mol H2). Cho dung dịch BaCl2 dư vào Z đến khi các phản ứng xảy ra hoàn toàn, thu được 93,2 gam kết tủa. Còn nếu cho Z phản ứng với NaOH thì lượng NaOH phản ứng tối đa là 0,935 mol. Giá trị của m gần giá trị nào nhất sau đây?
A. 2,5 B. 3,0 C. 1,0 D. 1,5
Câu 75: Khi nhúng thanh Mg có khối lượng m gam vào dung dịch hỗn hợp X chứa a mol Cu(NO3)2 và b mol HCl ta có đồ thị biểu diễn sự phụ thuộc của khối lượng Mg vào thời gian phản ứng được biểu diễn như hình vẽ dưới đây:
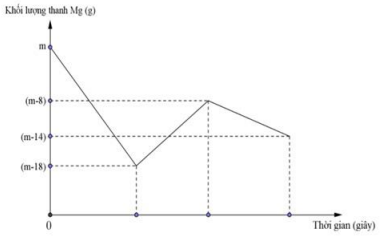
Sau khi phản ứng xảy ra hoàn toàn rút thanh Mg ra, thu được NO là sản phẩm khử duy nhất của N+5. Tỉ lệ a : b là
A. 1 : 10. B. 1 : 6.
C. 1 : 12. D. 1 : 8.
Câu 76: Đốt cháy hoàn toàn x mol một peptit X mạch hở được tạo thành từ amino axit no A chỉ chứa một nhóm –NH2 và một nhóm –COOH thì thu được b mol CO2 và c mol nước. Biết b – c = 3,5x. Số liên kết peptit trong X là
A. 9. B. 8. C. 10. D. 6.
Câu 77: Hỗn hợp X gồm peptit A mạch hở có công thức CxHyN5O6 và hợp chất B có công thức phân tử là C4H9NO2. Lấy 0,09 mol X tác dụng vừa đủ với 0,21 mol NaOH chỉ thu được sản phẩm là dung dịch gồm ancol etylic và a mol muối của glyxin, b mol muối của alanin. Nếu đốt cháy hoàn toàn 41,325 gam hỗn hợp X bằng lượng oxi vừa đủ thì thu được N2 và 96,975 gam hỗn hợp CO2 và H2O. Giá trị a : b gần nhất với
A. 0,50. B. 0,76. C. 1,30. D. 2,60.
Câu 78: Cho 33,1 gam hỗn hợp X gồm Fe3O4, Fe(NO3)2, Al tan hoàn toàn trong dung dịch chứa 210,8 gam KHSO4 loãng. Sau khi các phản ứng xảy ra hoàn toàn thu được dd Y chỉ chứa 233,3g muối sunfat trung hòa và 5,04 lít hh khí Z trong đó có 1 khí hóa nâu ngoài không khí. Biết tỉ khối của Z so với H2 là 23/9. Phần trăm khối lượng của Al trong hỗn hợp X là a%. a gần nhất với giá trị nào sau đây
A. 15 B. 30 C. 20 D. 25
Câu 79: Để thuỷ phân hết 7,612 gam hỗn hợp X gồm 2 este đơn chức và 2 este đa chức thì cần dùng vừa hết 80ml dung dịch KOH aM. Sau phản ứng, thu được hỗn hợp Y gồm các muối của các axit cacboxylic và các ancol. Đốt cháy hoàn toàn hỗn hợp Y thì thu được muối cacbonat, 4,4352 lít CO2 (đktc) và 3,168 gam H2O. Vậy a gần với giá trị nào sau đây nhất
A. 1,56 B. 1,42 C. 1,63 D. 1,25
Câu 80: Hỗn hợp X gồm 3,92 gam Fe, 16 gam Fe2O3 và m gam Al. Nung X ở nhiệt độ cao trong điều kiện không có không khí, thu được hỗn hợp chất rắn Y. Chia Y thành hai phần bằng nhau. Phần một tác dụng với dung dịch H2SO4 loãng (dư), thu được 4a mol khí H2. Phần hai phản ứng với dung dịch NaOH dư, thu được a mol khí H2. Biết các phản ứng đều xảy ra hoàn toàn. Giá trị của m là
A. 7,02. B. 3,51. C. 5,40. D. 4,05.
Đáp án đề thi thử THPT Quốc gia năm 2017 môn Địa lý
| 41, D 42, D 43, B 44, D 45, A 46, A 47, B 48, D 49, D 50, D | 51, D 52, B 53, D 54, C 55, D 56, B 57, B 58, C 59, A 60, B | 61, D 62, A 63, D 64, B 65, C 66, A 67, B 68, B 69, D 70, A | 71, B 72, C 73, C 74, D 75, A 76, B 77, C 78, A 79, C 80, A |







