Đề thi chọn học sinh giỏi môn Hóa học
Đề thi học sinh giỏi môn Sinh học lớp 12 năm học 2011 - 2012 tỉnh Long An là đề thi chọn học sinh giỏi cấp tỉnh lớp 12. Đề thi môn Hóa học có đáp án, giúp các em tự hệ thống và củng cố kiến thức cơ bản và nâng cao môn Hóa lớp 12, sẵn sàng cho các bài thi, bài kiểm tra sắp tới. Mời các em tham khảo.
Đề thi học sinh giỏi quốc gia lớp 12 THPT môn Toán
Đề thi học sinh giỏi môn Tiếng Anh lớp 12 tỉnh Thanh Hóa năm 2013 - 2014
Đề thi học sinh giỏi tỉnh Long An lớp 12 vòng 2 năm 2011 - 2012 môn Hóa học
|
SỞ GIÁO DỤC VÀ ĐÀO TẠO LONG AN (Đề thi chính thức) |
KỲ THI CHỌN HỌC SINH GIỎI LỚP 12 CẤP TỈNH - VÒNG 1 Ngày thi: 06 / 10 / 2011 Môn thi: HÓA HỌC Bảng: A Thời gian làm bài: 180 phút (Không kể thời gian phát đề) |
Cho khối lượng mol (mol/gam): H =1, N = 14, O = 16, Cl = 35,5, Cu = 64, Ca = 40,
Mg = 24, Al = 27, Fe = 56, C = 12, Na = 23, K = 39
Câu 1: (2 điểm)
Tổng số hạt proton của nguyên tử nguyên tố (A)và nguyên tử nguyên tố (D) là 42, (A) và (D) có cùng số thứ tự nhóm và ở 2 chu kì kế tiếp nhau trong bảng tuần hoàn, phân tử hợp chất tạobởi (A) với (D) là muối.
a.Xác định nguyên tố (A), (D); viết công thức hidroxit tương ứng với oxit cao nhất của (A), (D).
b.Từ phân tử hợp chất quan trọng của (A) và phân tử hợp chất của (D) hãy viết một phương trình phản ứng điều chế đơn chất (A) trong phòng thí nghiệm.
Câu 2: (2 điểm)
2.1. Cho một dung dịch chứa NH4Cl 0,1M và NH3 0,1M biết hằng số axit Ka của NH4+: 5.10-10, tính pH của dung dịch trên.
2.2. Thực nghiệm cho biết tốc độ của phản ứng: 2Ak + Bk -> Ck + Dk được tính theo biểu thức v= k.[A]2.[B]; trong đó k là hằng số tốc độ phản ứng, [A], [B] lần lượt là nồng độ mol/lit của A, B.Tốc độ của phản ứng trên tăng hoặc giảm bao nhiêu lần khi: tăng nồng độ A cũng như B lên 2 lần; giảm áp suất của hệ 3 lần.
Câu 3: (2 điểm)
3.1. Viết phương trình phản ứng dạng ion thu gọn cho mỗi trường hợp sau:
a. Dung dịch FeCl3 tác dụng với dung dịch Na2CO3.
b. Dung dịch HNO3 tác dụng với FexOy tạo chất khí NO.
3.2. Cho 200ml dung dịch chứa đồng thời K2CO3 0,001M và KOH 0,018M vào 200ml dung dịch chứa đồng thời HCl, HNO3, H2SO4 có cùng nồng độ 0,01M. Tìm pH của dung dịch thu được sau phản ứng.
Câu 4: (2 điểm)
4.1. Trộn lẫn 10,7g NH4Cl với 40g CuO trong một bình kín sau đó nung nóng để các phản ứng xảy ra hoàn toàn. Viết phương trình phản ứng xảy ra và tìm khối lượng của chất rắn khan sau phản ứng.
4.2. Không được dùng thêm hóa chất nào khác hãy trình bày cách nhận biết các chất rắn riêng biệt: NH4Cl, CaCO3, NaHCO3, NH4NO2, (NH4)3PO4, viết phương trình phản ứng hóa học đã dùng.
Câu 5: (4 điểm)
5.1. Cho hỗn hợp (A) gồm các chất CaCO3, MgCO3, Na2CO3, K2CO3 trong đó Na2CO3 và K2CO3 lần lượt chiếm a% và b% theo khối lượng của (A), biết trong điều kiện của thí nghiệm khi nung (A) chỉ có phản ứng phân hủy của CaCO3, MgCO3. Nung (A) một thời gian thu được chất rắn (B) có khối lượng bằng 80% khối lượng của (A) trước khi nung, để hòa tan vừa hết 10g (B) cần 150ml dung dịch HCl 2M. Nung (A) đến khối lượng không đổi thu được chất rắn (C). Viết toàn bộ các phản ứng đã xảy ra và lập biểu thức tính phần trăm khối lượng của (C) so với (A) theo a và b.
5.2. Hợp chất MX2 có trong tự nhiên. Hòa tan MX2 bằng dung dịch HNO3 dư một ít so với lượng cần tác dụng ta thu được dung dịch Y, khí NO2; dung dịch Y tác dụng với BaCl2 tạo kết tủa trắng không tan trong HNO3, dung dịch Y tác dụng với NH3 dư cho kết tủa màu nâu đỏ. Xác định công thức phân tử của MX2 và viết các phương trình ion trong các thí nghiệm nói trên.
Câu 6: (2 điểm)
6.1. Sắp xếp các chất sau theo chiều tăng dần từ trái qua phải (không giải thích):
a. Nhiệt độ sôi: H2O, H2S, CH3OH, C2H6, CH3F, O- O2NC6H4OH.
b.Lực axit: CH2=CHCOOH,CH=CCOOH, CH3CH2COOH, H2O, CH3CH2CH2OH, C6H5COOH.
6.2. Hai hợpchất hữu cơ (A), (B) có cùng công thức phân tử C7H7Cl và đều không tác dụng với dung dịch brom; hãy xác định công thức cấu tạo thu gọn của (A), (B), viết phương trình phản ứng của (A), (B) với NaOH dư (ghi rõ điều kiện phản ứng nếu có). Biết (A) phản ứng với NaOH cho muối hữu cơ, còn (B) tác dụng với NaOH cho sản phẩm hữu cơ (C) tác dụng được với Natri cho khí hidro.
Câu 7: (2 điểm)
Nhiệt phân 1mol hidrocacbon (A) cho 3 mol hỗn hợp khí và hơi (B). Đốt cháy 10,8g (B) rồi hấp thụ toàn bộ sản phẩm cháy vào dung dịch chứa 0,3 mol Ca(OH)2 và 0,35 mol NaOH sinh ra 20g kết tủa. Xác định công thức phân tử của (A), tỉ khối hơi của (B) so với hidro.
Câu 8: (4 điểm)
8.1.Viết phương trình phản ứng cho sơ đồ sau:
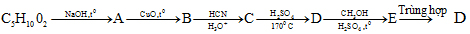
8.2. Đốt cháy hoàn toàn hợp chất hữu cơ (X) đơn chức cho CO2 và H2O; cho 27,45g (X) tác dụng hoàn toàn vừa đủ với NaOH ở điều kiện thích hợp thu được hỗn hợp sản phẩm (Y). Đốt cháy hoàn toàn (Y) thu được 23,85g chất rắn (Z) nguyên chất cùng hỗn hợp khí và hơi (T). Hấp thụ toàn bộ (T) vào dung dịch chứa 75,85g Ca(OH)2 sinh ra 70g kết tủa đồng thời khối lượng bình chứa tăng thêm 75,6g so với ban đầu. Hãy xác định công thức cấu tạo của hợp chất hũu cơ (X).









