Câu 1, 2, 3 phần bài tập bổ sung – Trang 84 Vở bài tập hoá 9
Giải câu 1, 2, 3 phần bài tập bổ sung – Trang 84 VBT hoá 9. Không nên ủ lò than trong phòng kín. Hãy giải thích và ...
Câu 1
Không nên ủ lò than trong phòng kín. Hãy giải thích và viết phương trình hóa học.
Phương pháp:
Khi đốt than, than sẽ phản ứng với oxi trong không khí sinh ra CO. CO là một chất khí cực độc.
Lời giải:
Không nên ủ lò than trong phòng kín vì trong phòng kín ít không khí. Than củ cháy trong điều kiện thiếu không khí sẽ tạo ra một loại khí cực độc là CO. Nạn nhân khi hít phải khí này nếu không được cấp cứu kịp thời sẽ gây tử vong.
Phương trình hóa học:
C+ O2 → CO2
C + CO2 → 2CO
Câu 2
Hãy ghép một chữ A, B, C, D với số 1, 2, 3, 4 hoặc 5 cho phù hợp
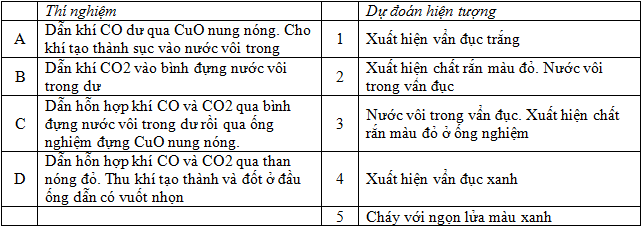
Phương pháp: Xem lại lí thuyết về tính chất các oxit của cacbon Tại đây
Lời giải:
Đáp án: A – 2 ; B – 1 ; C – 3 ; D – 5
Câu 3
Dẫn 0,336 lít khí CO2 (đktc) vào bình đựng 100ml dung dịch KOH 0,1M
a) Sản phẩm thu được sau phản ứng là:
A. KHCO3 B. K2CO3 C. K2CO3 và KOH D. KHCO3 và K2CO3
Hãy giải thích và viết phương trình hóa học, nếu có.
b) Tính nồng độ mol của các chất trong dung dịch sau phản ứng. Coi thể tích dung dịch thay đổi không đáng kể và khí CO2 hòa tan vào nước không đáng kể.
Phương pháp: Khi cho CO2 (hoặc SO2) tác dụng với dung dịch KOH đều xảy ra 3 khả năng tạo muối:
CO2 + 2KOH → K2CO3 + H2O (1)
CO2 + KOH → KaHCO3 (2)
Đặt T = nKOH/nCO2
- Nếu T ≥ 2 : chỉ tạo muối K2CO3
- Nếu T ≤ 1 : chỉ tạo muối KHCO3
- Nếu 1 < T < 2 : tạo cả muối KHCO3 và K2CO3
Lời giải:
a) n(CO2)= 0,336: 22,4 = 0,015 mol; nKOH = 0,1. 0,1 = 0,01 mol
Đáp án là: A
Phương trình hóa học:
KOH + CO2 → KHCO3
b) Nồng độ mol của các chất trong dung dịch sau phản ứng:
nKHCO3 = nKOH (do CO2 dư)= 0,01 mol
CM(KHCO3)= 0,01: 0,1 = 0,1 M
Search google: "từ khóa + timdapan.com" Ví dụ: "Câu 1, 2, 3 phần bài tập bổ sung – Trang 84 Vở bài tập hoá 9 timdapan.com"







