Đề thi thử tuyển sinh vào lớp 10 môn Hóa
Đề thi thử vào lớp 10 môn Hóa học trường THPT Chuyên Nguyễn Huệ, Hà Nội năm học 2017 - 2018 (Lần 1) có đáp án này, hi vọng sẽ giúp các bạn sẽ làm quen dần với cấu trúc đề thi, luyện giải nhiều các dạng bài tập và các câu hỏi lý thuyết. Chúc các bạn ôn thi thật hiểu quả và đạt kết quả cao trong kì thi sắp tới.
Đề thi thử vào lớp 10 THPT môn Hóa học trường THPT Chuyên Nguyễn Huệ, Hà Nội năm 2016 - 2017 (Lần 3)
Đề thi thử vào lớp 10 môn Vật lý trường THPT chuyên Nguyễn Huệ, Hà Nội năm học 2017 - 2018
|
TRƯỜNG THPT CHUYÊN NGUYỄN HUỆ |
KỲ THI THỬ VÀO LỚP 10 CHUYÊN LẦN 1 NĂM HỌC: 2016 – 2017 Môn: Hóa học (Đề gồm 4 câu 01 trang) Ngày thi: 26-02-2017 Thời gian làm bài: 120 phút (không kể thời gian giao đề) |
Câu 1: (2,75 điểm)
1. Giải thích ngắn gọn các vấn đề nêu sau:
a. Nguyên nhân gây mưa axit là gì?
b. Tại sao các khu đông dân cư không nên lập các nhà máy sản xuất đất đèn?
2. Có một hỗn hợp bột các oxit: K2O, MgO, BaO. Bằng phương pháp hóa học hãy tách riêng từng kim loại ra khỏi hỗn hợp các oxit trên.
3. Chọn 6 chất rắn khác nhau mà khi cho 6 chất đó lần lượt tác dụng với dung dịch H2SO4 đặc nóng đều thu được sản phẩm chỉ có Fe2(SO4)3 + SO2 + H2O. Viết các phương trình phản ứng minh hoạ.
Câu 2.( 1,75 điểm)
1. Hoàn thành các phương trình phản ứng của sơ đồ sau. Ghi rõ điều kiện (nếu có):
![]()
2. Đi từ các chất ban đầu là đá vôi, than đá và được dùng thêm các chất vô cơ cần thiết, hãy viết các phương trình phản ứng điều chế ra polivinyl clorua, 1,2- đicloetan.
Câu 3: (2,5 điểm)
1. Dung dịch X chứa a mol AlCl3 và 2a mol HCl. Rót từ từ dung dịch NaOH vào dung dịch X ta có đồ thị sau:
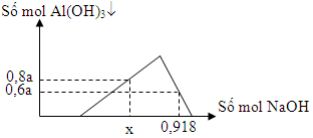
Tính giá trị của x?
2. Hoà tan hoàn toàn 8,24 gam hỗn hợp bột X gồm FexOy và Cu trong lượng dư dung dịch H2SO4 đặc nóng. Sau phản ứng thu được 0,784 lít khí SO2 (sản phẩm khí duy nhất, ở đktc) và dung dịch chứa 21,2 gam hỗn hợp hai muối sunfat.
Tìm công thức oxit sắt và tính khối lượng của mỗi chất trong hỗn hợp X .
3. Đốt 10,98 gam hỗn hợp X gồm Al và Mg trong bình đựng khí clo. Sau một thời gian phản ứng thu được 28,73 gam hỗn hợp Y gồm bốn chất rắn. Cho toàn bộ lượng hỗn hợp Y tan hết vào dung dịch HCl thì thu được V lít H2 (đktc). Dẫn V lít khí này đi qua ống đựng 40 gam CuO nung nóng, sau phản ứng thấy trong ống còn lại 36,16 gam chất rắn và chỉ có 75% lượng H2 đã phản ứng. Tính thành phần phần trăm theo khối lượng mỗi kim loại có trong hỗn hợp X.
Câu 4: (3 điểm)
1. Hỗn hợp A gồm C2H2 và H2. Cho 13,44 lít A đi qua ống đựng chất xúc tác Ni đun nóng, thu được 10,304 lít hỗn hợp khí B gồm 4 chất. Dẫn B đi chậm qua bình đựng nước brom dư cho phản ứng xảy ra hoàn toàn, thu được 7,84 lít hỗn hợp khí C. Biết rằng 1 mol A có khối lượng 8 gam và các thể tích khí đều đo ở điều kiện tiêu chuẩn. Hãy viết các phương trình phản xảy ra và tính thành phần phần trăm theo thể tích của các khí trong hỗn hợp A, B, C.
2. Một hỗn hợp gồm 2 hidrocacbon mạch hở CxH2x và CyH2y. Cứ 9,1 gam X làm mất màu vừa hết 40 gam brom trong dung dịch. Xác định công thức phân tử của 2 hidrocacbon đó. Biết trong X thành phần thể tích của chất có phân tử khối nhỏ hơn nằm trong khoảng từ 65% đến 75%.
3. Cho hidrocacbon X có công thức CnH2n+2 tác dụng với clo trong điều kiện có chiếu sáng thu được 16,65 gam hỗn hợp các dẫn xuất monoclo và điclo. Khí HCl bay ra được hấp thụ hoàn toàn bằng nước sau đó trung hòa bằng dung dịch NaOH thấy cần vừa đủ 250 ml dung dịch NaOH 1,2M. Tìm CTPT của X?
Cho: H = 1, C = 12, O = 16, Mg = 24, Al = 27, S = 32, Cl = 35,5, Fe = 56, Cu = 64, Br = 80
--------------------------- Hết ----------------------------
Đáp án đề thi thử tuyển sinh vào lớp 10 môn Hóa