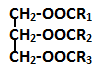Bài 2: Lipit
Video bài giảng
1. Khái niệm
Lipit là những hợp chất hữu cơ có trong tế bào sống, không hòa tan trong nước nhưng tan trong các dung môi hữu cơ không phân cực như: ete, cloroform, xăng dầu...
2. Chất béo
2.1. Khái niệm
- Lipit bao gồm chất béo, sáp, steroit, photpholipit… hầu hết chúng đều là các este phức tạp.
- Chất béo: là trieste của glixerol với các axit béo, là các axit monocacboxylic có số chẵn nguyên tử C (thường từ 12C đến 24C) không phân nhánh, được gọi chung là triglixerit.
- Công thức tổng quát của chất béo với R1, R2, R3 có thể giống nhau hoặc khác nhau.
- Một số axit béo thường gặp:
- Axit panmitic: C15H31COOH
- Axit stearic: C17H35COOH
- Axit oleic: C17H33COOH
- Axit linoleic: C17H31COOH
2.2. Tính chất vật lí của Lipit
- R1, R2, R3: không no ⇒ Chất béo lỏng (dầu thực vật)
Ví dụ: (C17H33COO)3C3H5
- R1, R2, R3: no ⇒ Chất béo rắn (mỡ động vật)
Ví dụ: (C17H35COO)3C3H5
3. Tính chất hóa học của Lipit
3.1. Phản ứng thủy phân
- Môi trường axit → axit béo + glixerol
(RCOO)3C3H5 + 3H2O → 3RCOOH + C3H5(OH)3
- Môi trường kiềm: (Phản ứng xà phòng hóa)
(RCOO)3C3H5 + 3NaOH → 3RCOONa + C3H5(OH)3
Muối Na, K của axit béo → gọi là xà phòng
Ví dụ: C17H35COONa, C17H35COOK, ...
3.2. Phản ứng cộng H2 của chất béo lỏng
(C17H33COO)3C3H5 + 3H2 → (C17H35COO)3C3H5 (đk: 175 - 190oC, xt: Ni)
- Chú ý: Chất béo không no sẽ bị oxh bởi không khí → peoxit, chất này bị phân hủy tạo thành các anđehit có mùi khó chịu và gây hại cho người ăn.
4. Vai trò chất béo
Chất béo → axit béo + glixerol
5. Bài tập Lipit - Cơ bản
Bài 1:
Khi thủy phân tristearin trong môi trường axit thu được sản phẩm là
Hướng dẫn:
Tristearin có công thức là: (C17H35COO)3C3H5
Ta có phản ứng thủy phân lipit trong môi trường axit thu được axit béo và glixerol
(C17H35COO)3C3H5 + 3H2O → 3C17H35COOH + C3H5(OH)3
Bài 2:
Thủy phân hoàn toàn 8,9 gam tristearin bằng dung dịch NaOH dư thì thu được m gam muối. Giá trị của m là
Hướng dẫn:
Cũng là Tristearin nhưng lại thủy phân trong môi trường bazơ (phản ứng xà phòng hóa)
(C17H35COO)3C3H5 + 3NaOH → 3C17H35COONa + C3H5(OH)3
0,01 mol → 0,03 mol
⇒ mmuối = 9,18g
Bài 3:
Để biến một số dầu thành mỡ rắn, hoặc bơ nhân tạo người ta thực hiện quá trình gì?
Hướng dẫn:
Dầu ý nói lipit ở trạng thái lỏng.Còn mỡ rắn hoặc bơ nhân tạo là nhắc đến lipit ở trạng thái rắn. Để chuyển đổi lipit từ trạng thái lỏng sang trạng thái rắn ta sử dụng quá trình Hidro hóa với điều kiện xúc tác Niken và nhiệt độ thích hợp.
Ví dụ: (C17H33COO)3C3H5 + 3H2 → (C17H35COO)3C3H5 (đk: 175 - 190oC, xt: Ni)
6. Bài tập Lipit - Nâng cao
Bài 1:
Thuỷ phân hoàn toàn 444 gam một lipit X thu được 46 gam glixerol (glixerin) và hai loại axit béo. Hai loại axit béo đó là
Hướng dẫn:
\({n_{glixerol}} = 0,5mol \Rightarrow {M_X} = 888\)
(R1COO)C3H5(R2COO)2 ⇒ R1 + 2R2 =715 ⇒ R1 =237 (C17H33) và R2 =239 (C17H35)
⇒ 2 axit béo đó là: axit oleic (C17H33COOH) và axit stearic (C17H35COOH)
Bài 2:
Đốt cháy hoàn toàn m gam 1 chất béo triglixerit cần 1,61 mol O2, sinh ra 1,14 mol CO2 và 1,06 mol H2O. Cho 7,088 gam chất béo tác dụng vừa đủ với dung dịch NaOH thì khối lượng muối tạo thành là
Hướng dẫn:
Bảo toàn khối lượng:
\({m_{lipit}} + {m_{{O_2}}} = {m_{C{O_2}}} + {m_{{H_2}O}}\)
\( \to {m_{lipit}} + 1,61.32 = 1,14.44 + 1,06.18\)
\( \to {m_{lipit}} = 17,72g\)
Bào toàn nguyên tố:
\({n_C} = {n_{C{O_2}}} = 1,14(mol)\)
\({n_H} = 2{n_{{H_2}O}} = 2,12{\mkern 1mu} (mol)\)
\(\begin{array}{l}
{n_{O\left( X \right)}} = 2{n_{C{O_2}}} + {n_{{H_2}O}} - 2{n_{{O_2}}}\\
= 2.1,14 + 1,06 - 2.1,61 = 0,12{\mkern 1mu} mol
\end{array}\)
X có công thức chung là (RCOO- là các gốc axit có thể khác nhau trong cùng 1 phân tử)
(RCOO)3C3H5 + 3NaOH → 3RCOONa + C3H5(OH)3
\(\begin{array}{l}
{n_X} = {n_{{C_3}{H_5}{{\left( {OH} \right)}_3}}} = 1/6.{n_{O\left( X \right)}} = 0,02{\mkern 1mu} mol\\
\to {n_{NaOH}} = 3{n_X} = 0,06{\mkern 1mu} mol
\end{array}\)
Xét trong 7,088g X thì
\({n_X} = 0,008\,mol \Rightarrow {n_{NaOH}} = 0,024\,mol\)
Bảo toàn khối lượng ta có:
\(\begin{array}{l}
m = {m_X} + {m_{NaOH}} - {m_{{C_3}{H_5}{{\left( {OH} \right)}_3}}}\\
= 7,312{\mkern 1mu} g
\end{array}\)
1. Khái niệm
Lipit là những hợp chất hữu cơ có trong tế bào sống, không hòa tan trong nước nhưng tan trong các dung môi hữu cơ không phân cực như: ete, cloroform, xăng dầu...
2. Chất béo
2.1. Khái niệm
- Lipit bao gồm chất béo, sáp, steroit, photpholipit… hầu hết chúng đều là các este phức tạp.
- Chất béo: là trieste của glixerol với các axit béo, là các axit monocacboxylic có số chẵn nguyên tử C (thường từ 12C đến 24C) không phân nhánh, được gọi chung là triglixerit.
- Công thức tổng quát của chất béo với R1, R2, R3 có thể giống nhau hoặc khác nhau.
- Một số axit béo thường gặp:
- Axit panmitic: C15H31COOH
- Axit stearic: C17H35COOH
- Axit oleic: C17H33COOH
- Axit linoleic: C17H31COOH
2.2. Tính chất vật lí của Lipit
- R1, R2, R3: không no ⇒ Chất béo lỏng (dầu thực vật)
Ví dụ: (C17H33COO)3C3H5
- R1, R2, R3: no ⇒ Chất béo rắn (mỡ động vật)
Ví dụ: (C17H35COO)3C3H5
3. Tính chất hóa học của Lipit
3.1. Phản ứng thủy phân
- Môi trường axit → axit béo + glixerol
(RCOO)3C3H5 + 3H2O → 3RCOOH + C3H5(OH)3
- Môi trường kiềm: (Phản ứng xà phòng hóa)
(RCOO)3C3H5 + 3NaOH → 3RCOONa + C3H5(OH)3
Muối Na, K của axit béo → gọi là xà phòng
Ví dụ: C17H35COONa, C17H35COOK, ...
3.2. Phản ứng cộng H2 của chất béo lỏng
(C17H33COO)3C3H5 + 3H2 → (C17H35COO)3C3H5 (đk: 175 - 190oC, xt: Ni)
- Chú ý: Chất béo không no sẽ bị oxh bởi không khí → peoxit, chất này bị phân hủy tạo thành các anđehit có mùi khó chịu và gây hại cho người ăn.
4. Vai trò chất béo
Chất béo → axit béo + glixerol
5. Bài tập Lipit - Cơ bản
Bài 1:
Khi thủy phân tristearin trong môi trường axit thu được sản phẩm là
Hướng dẫn:
Tristearin có công thức là: (C17H35COO)3C3H5
Ta có phản ứng thủy phân lipit trong môi trường axit thu được axit béo và glixerol
(C17H35COO)3C3H5 + 3H2O → 3C17H35COOH + C3H5(OH)3
Bài 2:
Thủy phân hoàn toàn 8,9 gam tristearin bằng dung dịch NaOH dư thì thu được m gam muối. Giá trị của m là
Hướng dẫn:
Cũng là Tristearin nhưng lại thủy phân trong môi trường bazơ (phản ứng xà phòng hóa)
(C17H35COO)3C3H5 + 3NaOH → 3C17H35COONa + C3H5(OH)3
0,01 mol → 0,03 mol
⇒ mmuối = 9,18g
Bài 3:
Để biến một số dầu thành mỡ rắn, hoặc bơ nhân tạo người ta thực hiện quá trình gì?
Hướng dẫn:
Dầu ý nói lipit ở trạng thái lỏng.Còn mỡ rắn hoặc bơ nhân tạo là nhắc đến lipit ở trạng thái rắn. Để chuyển đổi lipit từ trạng thái lỏng sang trạng thái rắn ta sử dụng quá trình Hidro hóa với điều kiện xúc tác Niken và nhiệt độ thích hợp.
Ví dụ: (C17H33COO)3C3H5 + 3H2 → (C17H35COO)3C3H5 (đk: 175 - 190oC, xt: Ni)
6. Bài tập Lipit - Nâng cao
Bài 1:
Thuỷ phân hoàn toàn 444 gam một lipit X thu được 46 gam glixerol (glixerin) và hai loại axit béo. Hai loại axit béo đó là
Hướng dẫn:
\({n_{glixerol}} = 0,5mol \Rightarrow {M_X} = 888\)
(R1COO)C3H5(R2COO)2 ⇒ R1 + 2R2 =715 ⇒ R1 =237 (C17H33) và R2 =239 (C17H35)
⇒ 2 axit béo đó là: axit oleic (C17H33COOH) và axit stearic (C17H35COOH)
Bài 2:
Đốt cháy hoàn toàn m gam 1 chất béo triglixerit cần 1,61 mol O2, sinh ra 1,14 mol CO2 và 1,06 mol H2O. Cho 7,088 gam chất béo tác dụng vừa đủ với dung dịch NaOH thì khối lượng muối tạo thành là
Hướng dẫn:
Bảo toàn khối lượng:
\({m_{lipit}} + {m_{{O_2}}} = {m_{C{O_2}}} + {m_{{H_2}O}}\)
\( \to {m_{lipit}} + 1,61.32 = 1,14.44 + 1,06.18\)
\( \to {m_{lipit}} = 17,72g\)
Bào toàn nguyên tố:
\({n_C} = {n_{C{O_2}}} = 1,14(mol)\)
\({n_H} = 2{n_{{H_2}O}} = 2,12{\mkern 1mu} (mol)\)
\(\begin{array}{l}
{n_{O\left( X \right)}} = 2{n_{C{O_2}}} + {n_{{H_2}O}} - 2{n_{{O_2}}}\\
= 2.1,14 + 1,06 - 2.1,61 = 0,12{\mkern 1mu} mol
\end{array}\)
X có công thức chung là (RCOO- là các gốc axit có thể khác nhau trong cùng 1 phân tử)
(RCOO)3C3H5 + 3NaOH → 3RCOONa + C3H5(OH)3
\(\begin{array}{l}
{n_X} = {n_{{C_3}{H_5}{{\left( {OH} \right)}_3}}} = 1/6.{n_{O\left( X \right)}} = 0,02{\mkern 1mu} mol\\
\to {n_{NaOH}} = 3{n_X} = 0,06{\mkern 1mu} mol
\end{array}\)
Xét trong 7,088g X thì
\({n_X} = 0,008\,mol \Rightarrow {n_{NaOH}} = 0,024\,mol\)
Bảo toàn khối lượng ta có:
\(\begin{array}{l}
m = {m_X} + {m_{NaOH}} - {m_{{C_3}{H_5}{{\left( {OH} \right)}_3}}}\\
= 7,312{\mkern 1mu} g
\end{array}\)