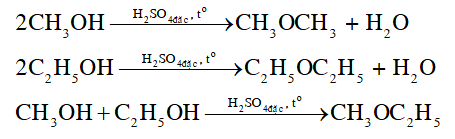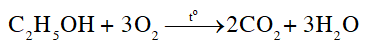Bài 16: Alcohol trang 107, 108, 109, 110, 111, 112, 113, 114, 115 Hóa học 11 Cánh diều
Chất X có trong thành phần của bia. Nếu lạm dụng, chất X là nguyên nhân của nhiều vấn đề xã hội như gây tai nạn giao thông, bạo lực gia đình, bệnh tật,... X là chất gì?
MĐ
Chất X có trong thành phần của bia. Nếu lạm dụng, chất X là nguyên nhân của nhiều vấn đề xã hội như gây tai nạn giao thông, bạo lực gia đình, bệnh tật,... X là chất gì?
Phương pháp giải:
Ethanol có nhiều trong đồ uống có cồn.
Lời giải chi tiết:
X là ethanol (C2H5OH).
CH 1
Cho các chất A, B, C, D và E có công thức cấu tạo như sau:
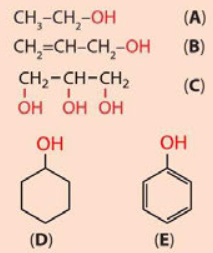
a) Hãy nhận xét đặc điểm chung về cấu tạo của các chất trên.
b) Hợp chất E có phải alcohol không?
Phương pháp giải:
Alcohol là những hợp chất hữu cơ trong phân tử có nhóm hydroxy (OH) liên kết trực tiếp với nguyên tử carbon no.
Lời giải chi tiết:
a) Cấu tạo của các hợp chất trên đều chứa nhóm –OH.
b) E không phải alcohol vì nhóm –OH của E liên kết với carbon trên vòng thơm, không liên kết với nguyên tử carbon no.
LT 1
Viết công thức cấu tạo, gọi tên thay thế và tên thông thường của các alcohol có công thức phân tử là C4H10O. Xác định bậc của alcohol trong mỗi trường hợp.
Phương pháp giải:
- Bậc của alcohol (bậc một, bậc hai và bậc ba) chính là bậc của nguyên tử carbon no liên kết với nhóm hydroxy.
- Tên thay thế: Nhóm hydroxy là nhóm thế gắn vào mạch chính của hydrocarbon. Việc đánh số thứ tự nguyên tử carbon trong mạch chính sao cho vị trí của nguyên tử carbon liên kết với nhóm hydroxy là nhỏ nhất.
+ Tên monoalcohol được gọi như sau:

+ Tên polyalcohol được gọi như sau:

Lời giải chi tiết:

LT 2
Một alcohol X có công thức phân tử là C2H6O2. Ở điều kiện thường, X là chất lỏng không màu, không mùi, tan tốt trong nước, có độ nhớt khá cao, có vị ngọt. Chất X được sử dụng rộng rãi làm chất chống đông và làm nguyên liệu trong sản xuất poly(ethylene terephtalate). Chất X có thể điều chế bằng cách oxi hoá trực tiếp ethylene bằng dung dịch potassium permanganate. Xác định công thức cấu tạo của X, gọi tên X theo tên thay thế và tên thông thường.
Phương pháp giải:
- Alcohol là những hợp chất hữu cơ trong phân tử có nhóm hydroxy (OH) liên kết trực tiếp với nguyên tử carbon no.
- Tên thay thế của polyalcohol được gọi như sau:

Lời giải chi tiết:
- X có công thức cấu tạo:

- Tên thay thế: ethane-1,2-diol.
- Tên thông thường: ethylene glycol.
LT 3
Vì sao ethanol có khả năng tan vô hạn trong nước?
Phương pháp giải:
Do tạo liên kết hydrogen tốt với nước, các alcohol chứa từ 1 đến 3 nguyên tử carbon trong phân tử tan vô hạn trong nước. Khi số nguyên tử carbon tăng lên thì độ tan của alcohol trong nước giảm dần.
Lời giải chi tiết:
Các phân tử ethanol tạo liên kết hydrogen với các phân tử nước nên ethanol có khả năng tan vô hạn trong nước.
LT 4
Cho các chất có công thức C2H6, C2H5Cl, C2H5OH, C6H5CH2OH và nhiệt độ sôi của chúng (không theo thứ tự) là 78,3 °C, -88,6 °C, 12,3 °C, 205 °C. Hãy dự đoán nhiệt độ sôi tương ứng với mỗi chất trên. Giải thích.
Phương pháp giải:
- Alcohol có nhiệt độ sôi cao hơn các hydrocarbon hoặc dẫn xuất halogen có phân tử khối tương đương. Nhiệt độ sôi và khối lượng riêng của các alcohol tăng dần khi phân tử khối tăng.
- Dẫn xuất halogen có nhiệt độ sôi cao hơn các hydrocarbon có phân tử khối tương đương.
Lời giải chi tiết:
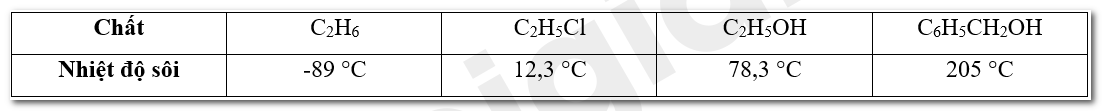
Giải thích: Ta có nhiệt độ sôi của các chất được sắp xếp theo thứ tự tăng dần như sau: C2H6, C2H5Cl, C2H5OH, C6H5CH2OH. Vì:
- Do tạo được liên kết hydrogen liên phân tử nên alcohol có nhiệt độ sôi cao hơn các hydrocarbon hoặc dẫn xuất halogen có phân tử khối tương đương.
- Nhiệt độ sôi của các alcohol tăng dần khi phân tử khối tăng.
- Dẫn xuất halogen có nhiệt độ sôi cao hơn các hydrocarbon có phân tử khối tương đương.
LT 5
Đun hỗn hợp methanol và ethanol với dung dịch sulfuric acid đặc ở nhiệt độ thích hợp thì thu được những ether nào? Viết phương trình hoá học của các phản ứng xảy ra.
Phương pháp giải:
Khi đun alcohol khác với dung dịch sulfuric acid đặc ở nhiệt độ thích hợp cũng thu được ether.
Lời giải chi tiết:
LT 6
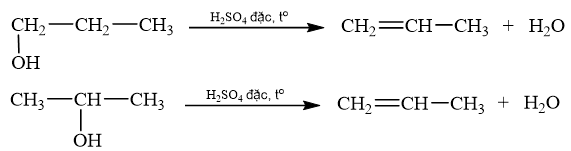
So sánh alkene sinh ra khi đun propan-1-ol và propan-2-ol với dung dịch sulfuric acid đặc. Viết phương trình hoá học của các phản ứng xảy ra.
Phương pháp giải:
Khi đun ethanol ở nhiệt 170 °C, có dung dịch sulfuric acid đặc làm xúc tác, sẽ thu được một chất khí làm mất màu nước bromine. Khí đó là ethylene.
Phản ứng này được dùng để điều chế ethylene trong phòng thí nghiệm. Các alkene khác cũng có thể được điều chế bằng phản ứng tương tự.
Lời giải chi tiết:
Khi đun propan-1-ol và propan-2-ol với dung dịch sulfuric acid đặc ta thu được 2 alkene giống nhau.
TN 1
Thí nghiệm 1. Đốt cháy ethyl alcohol
Chuẩn bị: Cồn 96%, đĩa sứ hoặc bát sứ.
Tiến hành: Nhỏ khoảng 1 - 2 mL cồn vào đĩa sứ hoặc bát sứ. Dùng que đóm châm lửa rồi tiến hành đốt cồn trong đĩa.
Yêu cầu: Quan sát, viết phương trình hoá học và giải thích hiện tượng xảy ra.
Phương pháp giải:
Các alcohol cháy, tỏa nhiều nhiệt.
Lời giải chi tiết:
- Hiện tượng: ethanol cháy tạo thành ngọn lửa màu vàng.
- Giải thích: ethanol cháy tốt trong không khí, khi cháy tỏa ra nhiều nhiệt.
- Phương trình:
CH 2
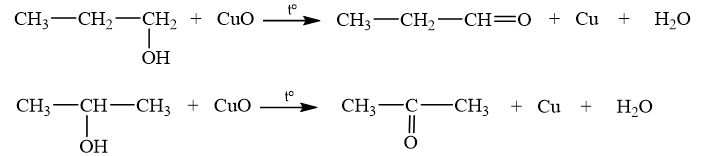
Cho biết sản phẩm sinh ra khi oxi hoá propyl alcohol và isopropyl alcohol bằng copper(II) oxide.
Phương pháp giải:
Alcohol bậc một bị oxi hoá bằng CuO sinh ra aldehyde.
Trong điều kiện tương tự, alcohol bậc hai bị oxi hoá sinh ra ketone.
Trong điều kiện trên, alcohol bậc ba không bị oxi hoá.
Lời giải chi tiết:
LT 7
Có ba ống nghiệm chứa các dung dịch sau: allyl alcohol, ethanol và glycerol. Bằng phương pháp hoá học, hãy nhận biết từng hóa chất chứa trong mỗi ống nghiệm.
Phương pháp giải:
Nhận biết allyl alcohol bằng phản ứng cộng của hydrocarbon không no.
Nhận biết glycerol bằng phản ứng hòa tan copper(II) hydroxide của polyalcohol có hai nhóm –OH liền kề.
Lời giải chi tiết:
- Đánh số thứ tự cho từng ống nghiệm. Trích các dung dịch làm mẫu thử, đánh số thứ tự tương ứng.
- Nhỏ vài giọt dung dịch sodium hydroxide và copper(II) sulfate vào từng mẫu thử, lắc đều ống nghiệm. Mẫu thử chứa glycerol sẽ xuất hiện kết tủa xanh lam rồi kết tủa tan dần tạo thành dung dịch xanh lam. Mẫu thử chứa allyl alcohol, ethanol sẽ xuất hiện kết tủa xanh lam nhưng kết tủa không bị tan.
CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4

- Cho vài giọt nước bromine vào hai mẫu thử chứa allyl alcohol, ethanol. Mẫu thử chứa allyl alcohol làm nước bromine mất màu vàng nhạt. Mẫu thử chứa ethanol không làm mất màu vàng nhạt của nước bromine.
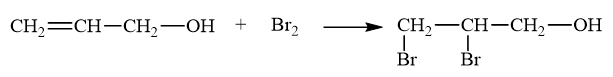
TN 2
Thí nghiệm 2. Hoà tan copper(II) hydroxide bằng glycerol
Chuẩn bị: dung dịch CuSO4 5%, dung dịch NaOH 20%, ethanol, glycerol; ống nghiệm.
Tiến hành: Chuẩn bị hai ống nghiệm, cho vào mỗi ống nghiệm có chứa 3 – 4 giọt dung dịch copper(II) sulfate 5% và 1 mL dung dịch sodium hydroxide 20%, lắc nhẹ. Tiếp tục nhỏ vào ống nghiệm thứ nhất 3 – 4 giọt ethanol, vào ống nghiệm thứ hai 3 – 4 giọt glycerol. Lắc nhẹ cả hai ống nghiệm.
Yêu cầu: Quan sát, mô tả hiện tượng và giải thích.
Phương pháp giải:
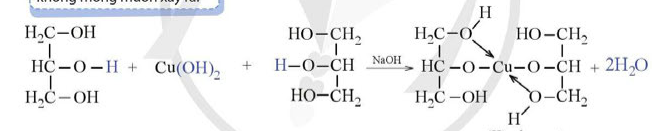
Glycerol hoà tan được copper(II) hydroxide tạo thành phức chất màu xanh lam, tan được trong nước.
Các polyalcohol có hai nhóm hydroxy liền kề như ethylene glycol cũng có phản ứng hoà tan copper(II) hydroxide tương tự như glycerol.
Lời giải chi tiết:
- Khi cho vào mỗi ống nghiệm: dung dịch copper(II) sulfate và dung dịch sodium hydroxide, lắc nhẹ, kết tủa màu xanh lam Cu(OH)2 xuất hiện.
CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4
- Nhỏ ethanol vào ống nghiệm thứ nhất, lắc nhẹ, không thấy có hiện tượng.
→ Ethanol không phản ứng với copper(II) hydroxide.
- Nhỏ glycerol vào ống nghiệm thứ hai, lắc nhẹ, kết tủa tan dần tạo thành dung dịch xanh lam.
→ Glycerol hoà tan được copper(II) hydroxide tạo thành phức chất màu xanh lam, tan được trong nước.
CH 3
Vì sao ethanol được sử dụng để làm nhiên liệu?
Phương pháp giải:
Đốt cháy ethanol tỏa nhiều nhiệt.
Lời giải chi tiết:
Đốt cháy ethanol tỏa nhiều nhiệt nên ethanol được sử dụng để làm nhiên liệu.
VD 1
Tìm hiểu và cho biết xăng E5 là gì. Vì sao xăng được trộn thêm một lượng ethanol được gọi là xăng sinh học?
Phương pháp giải:
Xăng E5 là xăng có 5% ethanol theo thể tích. Ethanol trộn vào xăng được điều chế từ chế phẩm sinh học.
Lời giải chi tiết:
- Xăng E5 là xăng có 5% ethanol theo thể tích.
- Xăng được trộn thêm 1 lượng ethanol lại được gọi là xăng sinh học vì lượng ethanol này được điều chế thông qua quá trình lên men các sản phẩm hữu cơ như tinh bột, cellulose … từ các nguyên liệu sinh học như ngô, lúa mì, đậu tương hoặc từ vỏ cây, bã mía (chất thải sản xuất)…
VD 2
Thực tế cho thấy việc lạm dụng rượu bia là nguyên nhân hàng đầu gây ra tai nạn giao thông. Em hãy chỉ ra các hậu quả của việc sử dụng rượu bia khi tham gia giao thông và cho biết ý kiến của cá nhân về việc này.
Phương pháp giải:
Ethanol có tác động đến hệ thống thần kinh và đặc biệt là não, làm phản ứng của cơ thể chậm đi. Nếu uống nhiều có thể bị choáng váng, bất tỉnh, thậm chí gây tử vong. Việc sử dụng lâu dài dẫn đến lạm dụng rượu và nghiện rượu. Hầu hết các quốc gia đều có luật quy định về việc sản xuất, bản và tiêu thụ đồ uống có cồn.
Lời giải chi tiết:
- Hậu quả của việc sử dụng rượu bia khi tham gia giao thông:
+ Giảm khả năng điều khiển phương tiện.
+ Tăng nguy cơ tai nạn giao thông.
+ Vi phạm luật giao thông.
+ Nếu uống nhiều có thể bị choáng váng, bất tỉnh, thậm chí gây tử vong.
- Ý kiến cá nhận về việc sử dụng rượu bia khi tham gia giao thông: Đã uống rượu bia thì không lái xe.
VD 3
Tìm hiểu và trình bày cụ thể quá trình sản xuất ethanol từ tinh bột. Liên hệ với quá trình sản xuất ethanol ở địa phương hoặc nơi em biết. Hãy phân tích ưu điểm và nhược điểm của phương pháp sản xuất này.
Phương pháp giải:
Ethanol được điều chế phổ biến bằng phương pháp lên men các nguyên liệu chứa nhiều tinh bột hoặc đường như ngũ cốc (gạo, ngô, khoai, sắn,...), quả chín (nho, anh đào,...).
Lời giải chi tiết:
- Ethanol được điều chế phổ biến bằng phương pháp lên men các nguyên liệu chứa nhiều tinh bột hoặc đường như ngũ cốc (gạo, ngô, khoai, sắn,...), quả chín (nho, anh đào,...). Quá trình lên men được tóm tắt như sau:
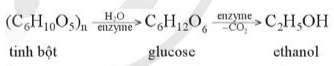
- Ở địa phương em, ethanol được điều chế bằng phương pháp lên men gạo nếp.
+ Ưu điểm: quá trình sản xuất đơn giản; nguyên liệu sinh học, thân thiện với môi trường.
+ Nhược điểm: hiệu suất sản xuất ethanol không cao, không đảm bảo được độ tinh khiết của rượu.
LT 8
Em hãy hoàn thiện các phản ứng hoá học điều chế glycerol từ propene.
Phương pháp giải:

Lời giải chi tiết:
Điều chế glycerol từ propene:
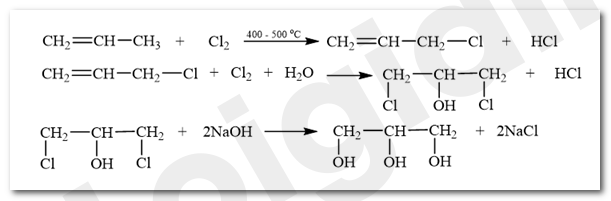
Bài 1
Viết công thức cấu tạo và gọi tên thay thế của các alcohol có cùng công thức phân tử C5H12O.
Phương pháp giải:
Tên thay thế của polyalcohol được gọi như sau:

Lời giải chi tiết:

Bài 2
Cho hai chất là butan-1-ol và butan-2-ol. Viết phương trình hoá học của phản ứng xảy ra khi:
a) Cho mỗi chất phản ứng với sodium.
b) Cho mỗi chất phản ứng với CuO, to.
c) Đun nóng mỗi chất với dung dịch H2SO4 đặc (tạo alkene).
Phương pháp giải:
a) Phản ứng thế nguyên tử hydrogen trong nhóm –OH.
b) Phản ứng oxi hóa không hoàn toàn alcohol bằng CuO. Alcohol bậc một bị oxi hoá bằng CuO sinh ra aldehyde, alcohol bậc hai bị oxi hoá sinh ra ketone.
c) Phản ứng tách nước tạo alkene.
Lời giải chi tiết:
a)
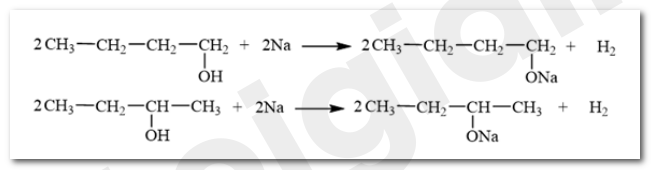
b)

c)
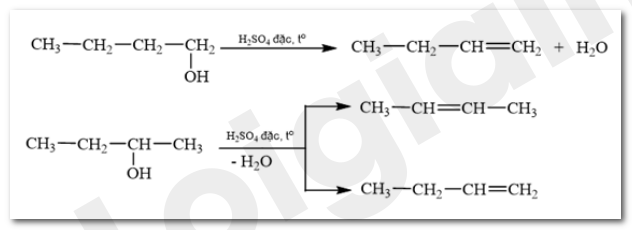
Bài 3
Ethanol có thể được điều chế bằng ba phương pháp theo sơ đồ sau đây:
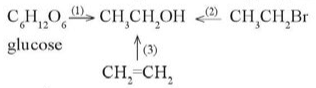
a) Viết phương trình hoá học của quá trình chuyển hoá trên.
b) Ethanol thu được bằng phương pháp nào ở trên được gọi là “ethanol sinh học”? Giải thích.
Phương pháp giải:
(1) Phương trình lên men glucose.
(2) Phản ứng thế nguyên tử halogen bằng nhóm –OH.
(3) Phản ứng cộng nước vào alkene.
Lời giải chi tiết:
a)
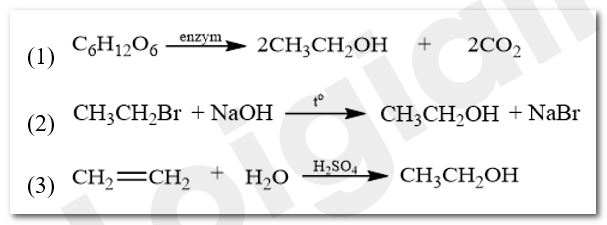
b) Ethanol thu được bằng phương pháp (1) được gọi là “ethanol sinh học”. Vì ethanol được điều chế thông qua quá trình lên men các sản phẩm hữu cơ như tinh bột từ các nguyên liệu sinh học như ngô, lúa mì, đậu tương hoặc từ vỏ cây, bã mía (chất thải sản xuất)…
Lý thuyết
Search google: "từ khóa + timdapan.com" Ví dụ: "Bài 16: Alcohol trang 107, 108, 109, 110, 111, 112, 113, 114, 115 Hóa học 11 Cánh diều timdapan.com"