Bài 35.11 trang 55 SBT hóa học 11
Giải bài 35.11 trang 55 sách bài tập hóa học 11. Cho 23 kg toluen tác dụng với hỗn hợp gồm 88 kg axit nitric 66% và ...
Đề bài
Cho 23 kg toluen tác dụng với hỗn hợp gồm 88 kg axit nitric 66% và 74 kg axit sunfuric 96%. Giả sử toluen được chuyển hoá hoàn toàn thành trinitrotoluen và sản phẩm này được tách hết khỏi hỗn hợp axit còn dư. Tính :
1. Khối lượng trinitrotuluen thu được.
2. Khối lượng hỗn hợp axit còn dư và nồng độ phần trăm của từng axit trong hỗn hợp đó.
Phương pháp giải - Xem chi tiết
1. Tính theo PTHH
2. Sử dụng công thức: \(C\% = \dfrac{{{m_{ct}}}}{{{m_{{\rm{dd}}}}}} \times 100\% \)
Lời giải chi tiết
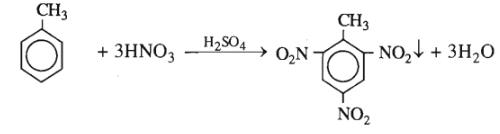
1. Số mol TNT = số mol toluen = \(\dfrac{{{{23.10}^3}}}{{92}}\) = 250 (mol).
Khối lượng TNT = \(\dfrac{{250.227}}{{{{10}^3}}} = {5675.10^{ - 2}}\) (kg).
2. Khối lượng hỗn hợp axit còn lại sau phản ứng :
23 + 88 + 74 - \({5675.10^{ - 2}}\) = \({12825.10^{ - 2}}\) (kg)
Khối lượng \(HN{O_3}\) trong đó : \(\dfrac{{88.66}}{{100}} - {3.25.10^{ - 2}}.63 = {1083.10^{ - 2}}\) (kg).
C% của \(HN{O_3}\) là : \(\dfrac{{{{1083.10}^{ - 2}}}}{{{{12825.10}^{ - 2}}}}\). 100% = 8,4%.
Khối lượng \({H_2}S{O_4}\) là : \(\dfrac{{74.96}}{{100}}\) = 71 (kg).
C% của \({H_2}S{O_4}\) là : \(\dfrac{{71}}{{{{12825.10}^{ - 2}}}}.100\% = 55,4\% .\)
Search google: "từ khóa + timdapan.com" Ví dụ: "Bài 35.11 trang 55 SBT hóa học 11 timdapan.com"







