Đề kiểm tra 45 phút (1 tiết) – Đề số 4 – Chương 4 – Hóa học 9
Đáp án và lời giải chi tiết đề thi kiểm tra 45 phút (1 tiết) – Đề số 4 – Chương 4 – Hóa học 9
Đề bài
I.Trắc nghiệm khách quan (4 điểm: mỗi 0,5 điểm)
Câu 1: Có thể phân biệt được 2 lít khí C2H4 và SO2 mà chỉ dùng dung dịch
A.Ca(OH)2 B.NaOH
C.NaCl D.Na2CO3.
Câu 2: Cho phản ứng 2CH4 \(\to\) C2H2 + 3H2 (15000C)
Để biết phản ứng đã xảy ra người ta
A.cho hỗn hợp sau phản ứng sục vào dung dịch brom, dung dịch brom mất màu.
B.đốt hỗn hợp sau phản nwgs, sẽ có phản ứng cháy và tỏa nhiều nhiệt.
C.quan sát thấy có hiện tượng sủi bọt do có khí H2 thoát ra.
D.so sánh thể tích hỗn hợp khí trước và sau khi đốt sẽ có sự giảm thể tích.
Câu 3: Số công thức cấu tạo có thể có của phân tử C3H8O là:
A.1 B.3
C.4 D.2
Câu 4: Một dãy các hợp chất có công thức cấu tạo viết gọn:
\(CH \equiv CH,CH \equiv C - C{H_3},\)\(\,CH \equiv C - C{H_2} - C{H_3},...\)
Một hidrocacbon mạch hở, phân tử có cấu tạo tương tự và có n nguyên tử cacbon sẽ có công thức phân tử là:
A.CnH2n+2 B.CnH2n
C.CnH2n-2 D.CnH2n-6.
Câu 5: Hợp chất hữu cơ X chứa các nguyên tố C, H, O trong đó thành phần phần trăm theo khối lượng C là 52,17% và hidro là 13,04%.
Biết khối lượng mol của X là 46 gam. Công thức phân tử của X là (H = 1, C = 12, O = 16)
A.C2H6O B.CH4O
C.C3H8O D.C2H6O2.
Câu 6: Khí C2H2 có lẫn khí CO2, SO2 và hơi H2O. Để thu được C2H2 tinh khiết có thể cho hỗn hợp qua
A.dung dịch KOH (dư), sau đó qua H2SO4 đặc.
B.dung dịch KOH (dư).
C.H2SO4 đặc.
D.H2SO4 đặc, sau đó qua dung dịch KOH (dư).
Câu 7: Đốt cháy hết hỗn hợp gồm metan và axetilen có thể tích 5,6 lít (đktc), cho sản phẩm qua một lượng dư dung dịch Ca(OH)2 thu được 40 gam CaCO3.
Thành phần % theo thể tích của axetilen trong hỗn hợp ban đâu là:
A.60% B.50%
C.40% D.30%
Câu 8: Từ CaC2, nước, người ta có thể điều chế trực tiếp chất nào trong các chất sau?
A.Etan (C2H6)
B.Etilen (C2H4)
C.Axetilen (C2H4)
D.Metan (CH4)
II.Tự luận (6 điểm)
Câu 9 (2,5 điểm): Viết các phương trình phản ứng:
a)Chứng tỏ benzen vừa có khả năng tham gia phản ứng thế, vừa có khả năng tham gia phản ứng cộng (ghi rõ điều kiện).
b)Đốt cháy hợp chất CnH2n+2. Nhận xét về tỉ lệ số mol giữa H2O và CO2 tạo ra.
Câu 10 (1,5 điểm): Tính thể tích etilen (đktc) cần dùng để điều chế 1kg polietilen.
Biết hiệu suất phản ứng 80% (cho H = 1, C = 12).
Câu 11 (2 điểm): Khi cho metan tác dụng với clo có chiếu sáng người ta thu được nhiều sản phẩm trong đó có chất X, với thành phần % khối lượng cacbon là 14,12%.
Xác định công thức phân tử của A (cho C = 12, H = 1, Cl =35,5).
Lời giải chi tiết
1. Đáp án
|
Câu |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
Đáp án |
A |
A |
B |
C |
A |
A |
A |
C |
2. Lời giải
I.Trắc nghiệm khách quan (4 điểm: mỗi câu 0,5 điểm)
Câu 1: (A)
Khí etilen không tác dụng với các dung dịch Ca(OH)2, NaOH, NaCl, Na2CO3
Khí SO2 chỉ tạo kết tủa với dung dịch Ca(OH)2
\(S{O_2} + Ca{(OH)_2} \to CaS{O_3} \downarrow + {H_2}O\)
Câu 2: (A)
Để biết phản ứng đã xảy ra người ta kiểm tra sự có mặt sản phẩm phản ứng:
Với: 2CH4 \(\to\) C2H2 + 3H2 (15000C)
Sản phẩm phản ứng là C2H2, H2. Chỉ có C2H2 làm mất ,àu dung dịch brom
Câu 3: (B)
Số công thức cấu tạo có thể có của phân tử C3H8O:
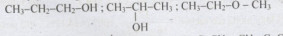
Câu 4: (C)
Dãy các chất \(CH \equiv CH,CH \equiv C - C{H_3},\)\(\,CH \equiv C - C{H_2} - C{H_3},...\) là những hợp chất mạch hở, phân tử có 1 liên kết 3 và đều thỏa mãn công thức chung CnH2n-2 (n nguyên dương lớn hơn bằng 2)
Câu 5: (A)
Thành phần phần trăm khối lượng của O:
\(\eqalign{ & 100 - (52,17 + 13,04) = 34,79\% \cr & {n_C}:{n_H}:{n_O} = {{52,17} \over {12}}:13,04:{{34,79} \over {16}} \cr&= 4,35:13,04:2,17 = 2:6:1 \cr} \)
\( \Rightarrow \) Công thức đơn giản nhất là C2H6O
\(M = (2.12+6+16)n = 46 \Rightarrow n = 1\)
Vậy công thức phân tử: C2H6O
Câu 6: (A)
Câu 7: (A)
Câu 8: (C)
CaC2 + 2H2O \(\to\) C2H2 + Ca(OH)2
II.Tự luận:
Câu 9:
a) Phản ứng thế của benzen: C6H6 + Br2 \(\to\) C6H5Br+ HBr
Phản ứng cộng của benzen: C6H6 + 3H2 \(\to\) C6H12
b) Đốt cháy hợp chất CnH2n+2
\({C_n}{H_{2n + 2}} + {{3n + 1} \over 2}{O_2} \to nC{O_2} + (n + 1){H_2}O(n \ge 1)\)
Số mol H2O luôn luôn lớn hơn số mol CO2
Câu 10:
\(\eqalign{ & nC{H_2} = C{H_2} \to - (C{H_2} - C{H_2}){ - _n} \cr & {m_{{C_2}{H_4}}} = {{1000.100} \over {80}} = 1250gam \cr & {n_{{C_2}{H_4}}} = {{1250} \over {28}} = 44,64mol \cr & {V_{{C_2}{H_4}}} = {{1250.22,4} \over {28}} = 1000lit \cr} \)
Câu 11:
\(\eqalign{ & C{H_4} + xC{l_2} \to C{H_{4 - x}}C{l_x} + xHCl \cr & \% {m_C} = {{12} \over {16 + 34,5x}}.100\% = 14,12\% \cr & 225,92 + 487,14x = 1200\cr& \Rightarrow 487,14x = 1200 - 225,92 = 974,08 \cr & \Rightarrow x = 2 \cr} \)
Công thức phân tử của X là CH2Cl2
Search google: "từ khóa + timdapan.com" Ví dụ: "Đề kiểm tra 45 phút (1 tiết) – Đề số 4 – Chương 4 – Hóa học 9 timdapan.com"







