Đề kiểm tra 15 phút – Đề số 7 – Chương 4 – Hóa học 9
Đáp án và lời giải chi tiết đề thi kiểm tra 15 phút – Đề số 7 – Chương 4 – Hóa học 9
Đề bài
Câu 1 (1 điểm): Trong các chất sau:
\(C{H_3}OH(1),NaHC{O_3}(2),KCN(3),C{H_3}COOH(4),\)\(\,{C_6}{H_6}(5),Ca{C_2}(6).\)
Các chất hữu cơ là:
A.(3), (4), (5), (6).
B.(1), (2), (5), (6).
C.(1), (2), (3), (4).
D.(1), (4), (5).
Câu 2 (1 điểm): Trong C2H4 cứ có 6 gam C thì khối lượng H sẽ là:
A.2,2 gam B.1,0 gam
C.1,2 gam D.1,5 gam.
Câu 3 (1 điểm): Công thức nào sau đây là công thức cấu tạo của chất có công thức phân tử là C3H8O?
A.CH3- CH2 – CH2 – OH.
B.CH3- O – CH2 – CH3
C.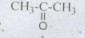
D.Cả A và B.
Câu 4 ( 1 điểm): Dung dịch brom có màu da cam khi dẫn khí etilen đi qua, hiện tượng quan sát được là:
A.có chất lỏng màu nâu xuất hiện.
B.màu da cam của dung dịch phai dần.
C.có chất khí thoát ra.
D.không thấy có sự thay đổi nào.
Câu 5 (1 điểm): Đốt cháy hoàn toàn 2,6 gam C2H2 thì khối lượng CO2 và H2O thu được là
A.8,8 gam CO2, 1,8 gam H2O.
B.4,4 gam CO2, 1,8 gam H2O.
C.4,4 gam CO2, 4,4 gam H2O.
D.1,8 gam CO2, 8,8 gam H2O.
Câu 6 (2 điểm): Nhận biết các khí CO2, C2H4, CH4 đựng trong các bình riêng biệt không ghi nhãn, người ta phải dùng dung dịch
A.brom
B.nước vôi trong
C.NaCl
D.brom và dung dịch nước vôi trong.
Câu 7 (1 điểm): Khi đốt cháy chất hữu cơ có công thức phân tử: CnH2n-2 thì tỉ lệ số mol CO2 và H2O sinh ra:
A.bằng 1
B.bé hơn 1
C.lớn hơn 1
D.không xác định được.
Câu 8 (1 điểm): Đốt cháy hoàn toàn 3 gam hợp chất hữu cơ X thu được 4,4 gam CO2 và 1,8 gam H2O. Tỉ khối hơi của X là (H = 1, C = 12, O = 16)
A.C2H4O2 B.C4H12
C.CH2O D.C3H8O.
Lời giải chi tiết
1.Đáp án
|
Câu |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
Đáp án |
D |
B |
D |
B |
A |
D |
C |
A |
2.Lời giải
Câu 1: (D)
NaHCO3(2), KCN (3), CaC2 (6) không phải là chất hữu cơ.
Câu 2: (B)
Trong 1 mol C2H4 cứ có 24 gam C thì có 4 gam H
\(\Rightarrow \) với 6 gam C thì \({m_H} = {{6.4} \over {24}} = 1gam\)
Câu 3: (D)
CH3 – CH2 – CH2 – OH, CH3 – O – CH2 – CH3 đều có cùng công thức phân tử C3H8O.
Câu 4: (B)
Do sản phẩm phản ứng là C2H4Br2 không màu, tan trong dung dịch nên không có chất khí được tạo thành.
Câu 5: (A)
\(\eqalign{ & 2{C_2}{H_2} + 5{O_2} \to 4C{O_2} + 2{H_2}O \cr & {n_{{C_2}{H_2}}} = {{2,6} \over {26}} = 0,1mol \cr&\Rightarrow {n_{C{O_2}}} = 0,2mol \cr&\Rightarrow {m_{C{O_2}}} = 8,8gam. \cr & {n_{{H_2}O}} = 0,1mol \Rightarrow {m_{{H_2}O}} = 1,8gam. \cr} \)
Câu 6: (D)
C2H4 làm phai màu dung dịch brom, CO2 tạo kết tủa với dung dịch nước vôi trong.
Câu 7: (C)
\(\eqalign{ & {C_n}{H_{2n - 2}} + {{3n - 1} \over 2}{O_2} \to nC{O_2} + (n - 1){H_2}O \cr & {{{n_{C{O_2}}}} \over {{n_{{H_2}O}}}} = {n \over {n - 1}} > 1 \cr} \)
Câu 8: (A)
\(\eqalign{ & {n_{C{O_2}}} = {{4,4} \over {44}} = 0,1mol,\cr&{n_{{H_2}O}} = {{1,8} \over {18}} = 0,1mol \cr & \Rightarrow {m_C} = 1,2gam,{m_H} = 0,2gam \cr&\Rightarrow {m_O} = 3 - (1,2 + 0,2) = 1,6gam \cr & \Rightarrow nC:nH:nO = 1:2:1. \cr} \)
Công thức đơn giản nhất là CH2O
Công thức phân tử: (CH2O)n \( \Rightarrow M = 30n = 60 \Rightarrow n = 2.\)
Công thức phân tử là C2H4O2.
Search google: "từ khóa + timdapan.com" Ví dụ: "Đề kiểm tra 15 phút – Đề số 7 – Chương 4 – Hóa học 9 timdapan.com"







